题目内容
6.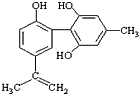 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )| A. | 滴入酸性高锰酸钾溶液振荡,紫色褪去,能证明其结构中存在碳碳双键 | |
| B. | 1mol该物质分别与浓溴水和H2反应时最多消耗溴水和H2分别为4mol和7mol | |
| C. | 该物质与苯酚属于同系物,遇FeCl3溶液呈紫色 | |
| D. | 该分子中的所有碳原子不可能共平面 |
分析 该有机物中含有苯环、碳碳双键、酚羟基,具有苯、烯烃和酚的性质,能发生加成反应、取代反应、氧化反应、加聚反应、显色反应等,据此分析解答.
解答 解:A.碳碳双键和连接苯环的甲基都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以不能用酸性高锰酸钾溶液检验碳碳双键,故A错误;
B.能和浓溴水反应的有苯环酚羟基邻对位氢原子、碳碳双键,能和氢气发生加成反应的是苯环和碳碳双键,所以1mol该物质分别与浓溴水和H2反应时最多消耗溴水和H2分别为4mol和7mol,故B正确;
C.该物质中含有两个苯环、3个酚羟基和碳碳双键,所以与苯酚不是同系物,故C错误;
D.苯环上所有原子共平面、连接碳碳双键两端的原子共平面,所以该分子中的所有碳原子可能共平面,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系是解本题关键,注意酚和溴发生取代反应位置,易错选项是D.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
16.已知:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1)△H1,
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(1)△H3;
2H2(g)+O2(g)=2H2O(g)△H4
CO(g)+2H2(g)=CH3OH(g)△H5
下列关于上述反应焓变的判断正确的是( )
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(1)△H3;
2H2(g)+O2(g)=2H2O(g)△H4
CO(g)+2H2(g)=CH3OH(g)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1<0,△H2>0 | B. | 0>△H3>△H4 | ||
| C. | 2△H5+△H1>0 | D. | △H1=△H2+△H3-2△H5 |
14.BHTCButylated Hydroxy Toluene)是一种常用的食品抗氧化剂,合成方法有如下两种:
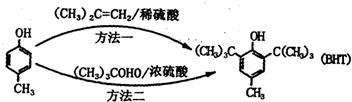
下列说法不正确的是( )

下列说法不正确的是( )
| A. | BHT在水中的溶解度小于苯酚 | |
| B. | 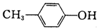 与BHT互为同系物 与BHT互为同系物 | |
| C. | 1molBHT可与含有2molBr2的浓溴水发生取代反应 | |
| D. | 方法一的原子利用率为100% |
18.下列有关电化学原理的说法中,不正确的是( )
| A. | 镀锌铁制品镀层受损后,铁制品也不容易生锈 | |
| B. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH | |
| C. | 粗铜精炼时,电镀液中的c(Cu2+)保持不变 | |
| D. | 将钢闸门与直流电源的负极相连,可降低钢闸门腐蚀速率 |
15.X、Y、Z、W是原子序数依次增大的不同主族短周期元素,其中两种为金属元素,X原子的最外层电子数与次外层电子数相等,X与W、Y与Z这两对原子的最外层电子数之和均为9.下列说法正确的是( )
| A. | Y的简单离子半径大于W的简单离子半径 | |
| B. | Z的氧化物对应水化物为强酸 | |
| C. | XW2熔沸点较低,可能是共价化合物 | |
| D. | 工业制Y可以电解熔融的YW3制得 |
16.下列对水体污染物的处理方法中,不正确的是( )
| A. | 含盐酸的酸性废水,用中和法处理 | |
| B. | 含Cu2+、Fe3+的废水,用沉淀法处理 | |
| C. | 混凝法是处理污水中细小悬浮颗粒污染物的常用方法 | |
| D. | 含有重金属离子的废水用明矾处理 |
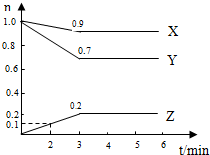 某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线
某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线 氮及其化合物与人类生产、生活息息相关.回答下列问题:
氮及其化合物与人类生产、生活息息相关.回答下列问题: