题目内容
17.用0.1000mol•L-1标准NaOH溶液测定食醋中醋酸的含量,下列说法正确的是( )| A. | 酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2-3次 | |
| B. | 可使用酚酞或甲基橙作指示剂 | |
| C. | 滴定过程中眼睛应始终注视滴定管内液面变化 | |
| D. | 读取标准溶液的刻度时,滴定前平视,滴定后仰视,测定结果偏高 |
分析 A.根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断误差;
B.醋酸与氢氧化钠恰好反应时生成醋酸钠,醋酸钠为强碱弱酸盐,水解呈碱性,选择碱性变色范围内的指示剂;
C.滴定过程中眼睛需要观察锥形瓶中溶液颜色变化,以判定滴定终点;
D.根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断误差.
解答 解:A.锥形瓶用待测液润洗,待测液的物质的量偏大,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,测定结果偏大,故A错误;
B.用0.1000mol•L-1标准NaOH溶液测定食醋中醋酸,醋酸钠为强碱弱酸盐,水解呈碱性,可用酚酞作指示剂,不能用甲基橙作指示剂,故B错误;
C.滴定时已经应该观察锥形瓶中溶液颜色变化,以便及时判断滴定终点,故C错误;
D.读取标准溶液的刻度时,滴定前平视,滴定后仰视,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,测定结果偏大,故D正确;
故选D.
点评 本题考查了中和滴定操作方法及误差分析,题目难度中等,注意掌握选用指示剂的方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol (CH2)6N4H+与l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,
某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取1.500g样品,加水溶解,配成250mL溶液.
步骤Ⅱ用酸式滴定管量取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液.用0.1010mol•L-1的NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据实验步骤填空:
①步骤Ⅰ中用到的主要玻璃仪器有250mL容量瓶、胶头滴管、烧杯、玻璃棒;
②步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取,则测得样品中氮质量分数偏低(填“偏高”、“偏低”或“无影响”,下同).锥形瓶用蒸馏水洗涤后,水未倒尽,则对滴定时用去NaOH标准溶液的体积无影响.滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则测得样品中氮质量分数偏低.
③滴定时边滴边摇动锥形瓶,眼睛应观察B
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红色.
(2)滴定结果如表所示:
则消耗NaOH标准溶液的体积平均为20.00mL,该样品中氮的质量分数为18.85%.
某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取1.500g样品,加水溶解,配成250mL溶液.
步骤Ⅱ用酸式滴定管量取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液.用0.1010mol•L-1的NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据实验步骤填空:
①步骤Ⅰ中用到的主要玻璃仪器有250mL容量瓶、胶头滴管、烧杯、玻璃棒;
②步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取,则测得样品中氮质量分数偏低(填“偏高”、“偏低”或“无影响”,下同).锥形瓶用蒸馏水洗涤后,水未倒尽,则对滴定时用去NaOH标准溶液的体积无影响.滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则测得样品中氮质量分数偏低.
③滴定时边滴边摇动锥形瓶,眼睛应观察B
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红色.
(2)滴定结果如表所示:
| 滴定次数 | 待测溶液体积/ml[ | 标准NaOH溶液体积读数(ml) | |
| 滴定前/ml | 滴定后/ml | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.30 | 22.30 |
12.用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.称量时,样品可放在A(填编号字母)称量.
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定时,用0.20mol•L-的盐酸来滴定待测液,不可选用B(填编号字母)作指示剂.
A.甲基橙 B.石蕊 C.酚酞
(3)根据下表数据,计算被测烧碱溶液的物质的量浓度是0.4000mol/L,烧碱样品的纯度是97.56%
(4)在铁架台上垫一张白纸,其目的是便于观察锥形瓶内液体颜色的变化,减小滴定误差
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果偏高
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果无影响.
(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.称量时,样品可放在A(填编号字母)称量.
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定时,用0.20mol•L-的盐酸来滴定待测液,不可选用B(填编号字母)作指示剂.
A.甲基橙 B.石蕊 C.酚酞
(3)根据下表数据,计算被测烧碱溶液的物质的量浓度是0.4000mol/L,烧碱样品的纯度是97.56%
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果偏高
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果无影响.
4.用如图所示装置能达到有关实验目的是( )
| A. | 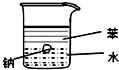 证明密度ρ(苯)<ρ(钠)<ρ(水) | B. | 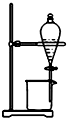 分离酒精和四氯化碳 | ||
| C. | 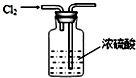 干燥Cl2 | D. | 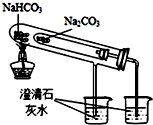 比较NaHCO3和Na2CO3的热稳定性 |
 ,Z元素在周期表中的位置为第三周期第ⅥⅠA族族,能否用下面的反应证明Z的非金属性比碳强:2HCl+Na2CO3=NaCl+H2O+CO2↑否(填“能”或“否”)
,Z元素在周期表中的位置为第三周期第ⅥⅠA族族,能否用下面的反应证明Z的非金属性比碳强:2HCl+Na2CO3=NaCl+H2O+CO2↑否(填“能”或“否”)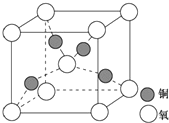 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:CuFeS2$→_{800℃}^{O_{2}}$Cu2S$→_{△①}^{O_{2}}$Cu2O$→_{②}^{Cu_{2}S}$Cu
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:CuFeS2$→_{800℃}^{O_{2}}$Cu2S$→_{△①}^{O_{2}}$Cu2O$→_{②}^{Cu_{2}S}$Cu