题目内容
15.表是25℃时某些弱酸的电离平衡常数,下列说法正确的是( )| 化学式 | CH3COOH | HClO | H2CO3 |
| Ka | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时c(CH3COOH):c(CH3COO-)=9:5 | |
| C. | 少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大 | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaClO(aq)中离子总数大小:N前<N后 |
分析 A.酸的电离常数越大,则酸根离子的水解程度越小;
B.根据电离常数计算;
C.少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应;
D.NaClO水解程度较大,溶液中氢离子浓度较小,结合电荷守恒判断.
解答 解:A.醋酸的电离常数大于次氯酸,所以醋酸的水解程度小于次氯酸,醋酸钠和次氯酸钠都是强碱弱酸盐,其混合溶液呈碱性,所以相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+),故A错误;
B.CH3COOH的电离常数为1.8×10-5,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,则$\frac{c({H}^{+})c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=1.8×10-5,c(CH3COOH):c(CH3COO-)=10-5:1.8×10-5=5:9,故B错误;
C.氯水中存在Cl2+H2O?H++Cl-+HClO,少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应,则平衡正向移动,c(HClO)增大,故C正确;
D.HClO酸性较弱,NaClO水解程度较大,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-)、c(Na+)+c(H+)=c(OH-)+c(ClO-),由于NaClO水解程度较大,溶液中氢离子浓度较小,且两溶液钠离子浓度相等,所以CH3COONa溶液中离子总数大于NaClO溶液,即N前>N后,故D错误.
故选C.
点评 本题考查电解质的强弱与电离常数的关系,为高频考点,侧重于学生的分析能力和计算能力的考查,明确酸的电离常数与酸的强弱、酸根离子水解能力的关系是解本题关键,难度中等.

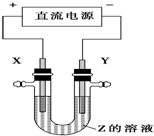 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 外加电流的阴极保护法中,Y是待保护金属 |
| A. | CH4和C2H4 | B. | CH4和C2H6 | C. | C2H4和C2H6 | D. | C3H4和C3H6 |
| A. | 加热 | B. | 加NaOH | C. | 通CO2气体 | D. | 加盐酸 |
| A. | CH2═CH-CN | B. | CH2═CH-CH═CH2 | C. | 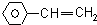 | D. | 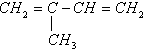 |
| A. | A、C两种元素仅可组成化学式为CA3的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F>C>D | |
| D. | 元素的非金属性由强到弱的顺序是D>C>F>B |
| 选项 | 操作 | 现象 | 结论 |
| A | 将20mL2mol/L的NaOH溶液缓缓地倒入20mL2mol/L的盐酸中,边加边搅拌,测定反应前后溶液温度的变化 | 温度升高 | 释放出的热量就是中和热 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小段镁带和一小块铝分别放在同体积、同浓度的盐酸中 | 都有气泡产生,镁带产生气泡更快 | 镁比铝活泼 |
| D | 将少量氯气通入到NaBr溶液中 | 溶液变成橙红色 | 氯气溶于水呈现橙红色 |
| A. | A | B. | B | C. | C□D.D |
| A. | 某无色溶液中:Al3+、Cu2+、SO${\;}_{4}^{2-}$、Cl- | |
| B. | 由水离子的c(H+)=1×10-12mol•L-1的溶液中:Ba2+、K+、Cl-、NO${\;}_{3}^{-}$ | |
| C. | c(OH-)/c(H+)═1012的溶液中:Na+、Mg2+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 含有大量HCO${\;}_{3}^{-}$的溶液中:NH${\;}_{4}^{+}$、Al3+、Ca2+、Cl- |