题目内容
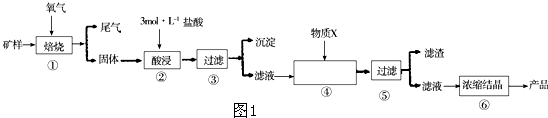
碘化钠是常用的分析试剂,还用于医疗、照相业.工业上用铁屑还原法制备NaI,其主要流程如下,

请回答问题:
已知:NaI易被空气氧化;反应②为:3Fe+IO3-+3H2O→3Fe (OH)2↓+I-
(1)实验室灼烧Fe(OH)2主要在 进行(填仪器名称);灼烧后的副产品是 (写化学式).
(2)判断①中碘单质是否完全反应的实验方法是 ;
(3)实验室配制一定量10%NaOH溶液,其操作步骤是 .
(4)测定产品中NaI含量的方法是:
a.称取3.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用0.1000mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19.00mL.
①测定过程所需仪器在使用前需要检查是否漏液的有 .
②该样品中NaI的质量分数为 .
③若测定结果偏低,试分析可能的原因(任写两条): 、 .

请回答问题:
已知:NaI易被空气氧化;反应②为:3Fe+IO3-+3H2O→3Fe (OH)2↓+I-
(1)实验室灼烧Fe(OH)2主要在
(2)判断①中碘单质是否完全反应的实验方法是
(3)实验室配制一定量10%NaOH溶液,其操作步骤是
(4)测定产品中NaI含量的方法是:
a.称取3.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用0.1000mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19.00mL.
①测定过程所需仪器在使用前需要检查是否漏液的有
②该样品中NaI的质量分数为
③若测定结果偏低,试分析可能的原因(任写两条):
考点:探究物质的组成或测量物质的含量,制备实验方案的设计
专题:实验题
分析:由制备流程可知,碘与NaOH溶液反应生成NaI、NaIO3,加入Fe与NaIO3发生氧化还原反应生成NaI、氢氧化铁,过滤后得到的NaI溶液经蒸发浓缩、冷却结晶可得到NaI,氢氧化铁灼烧分解生成氧化铁.
(1)灼烧固体在坩埚中进行,氢氧化铁受热分解生成氧化铁和水;
(2)根据淀粉遇碘变蓝色判断;
(3)配制一定质量分数的溶液步骤为:计算、称量、溶解;
(4)测定产品中NaI含量,滴加硝酸银,根据硝酸银的物质的量可确定质量分数,注意仪器的使用方法.
(1)灼烧固体在坩埚中进行,氢氧化铁受热分解生成氧化铁和水;
(2)根据淀粉遇碘变蓝色判断;
(3)配制一定质量分数的溶液步骤为:计算、称量、溶解;
(4)测定产品中NaI含量,滴加硝酸银,根据硝酸银的物质的量可确定质量分数,注意仪器的使用方法.
解答:
解:由制备流程可知,碘与NaOH溶液反应生成NaI、NaIO3,加入Fe与NaIO3发生氧化还原反应生成NaI、氢氧化铁,过滤后得到的NaI溶液经蒸发浓缩、冷却结晶可得到NaI,氢氧化铁灼烧分解生成氧化铁;
(1)灼烧固体在坩埚中进行,氢氧化铁受热分解生成氧化铁和水,氧化铁可作红色颜料,故答案为:坩埚;Fe2O3;
(2)淀粉遇碘变蓝,反应后加淀粉无现象即可说明反应结束,则判断反应中碘是否反应完全的方法为取少量反应后的溶液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已反应完全;反之,碘未反应完全,故答案为:取少量反应后的混合液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已完全反应,反之则未完全反应;
(3)配制一定质量分数的溶液步骤为:计算、称量、溶解,故答案为:计算、称量、溶解;
(4)①配制溶液用250mL容量瓶,滴定用酸式滴定管,都应检查是否漏液,故答案为:250 mL容量瓶、酸式滴定管;
②n(NaI)=n(AgNO3)=0.1mol/L×0.019L=0.0019mol,
则3.000g样品中含有n(NaI)=0.019mol,m(NaI)=0.019mol×150g/mol=2.85g,
ω(NaI)=
×100%=95.00%,
故答案为:95.00%;
③若用上述方法测定产品中NaI的质量分数偏低,可考虑样品的原因,两种情况,一是样品被氧化,二是样品吸水,
故答案为:样品在空气中被氧化;样品在空气中吸水.
(1)灼烧固体在坩埚中进行,氢氧化铁受热分解生成氧化铁和水,氧化铁可作红色颜料,故答案为:坩埚;Fe2O3;
(2)淀粉遇碘变蓝,反应后加淀粉无现象即可说明反应结束,则判断反应中碘是否反应完全的方法为取少量反应后的溶液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已反应完全;反之,碘未反应完全,故答案为:取少量反应后的混合液于试管中,滴入几滴淀粉溶液,若溶液未变蓝,则证明碘已完全反应,反之则未完全反应;
(3)配制一定质量分数的溶液步骤为:计算、称量、溶解,故答案为:计算、称量、溶解;
(4)①配制溶液用250mL容量瓶,滴定用酸式滴定管,都应检查是否漏液,故答案为:250 mL容量瓶、酸式滴定管;
②n(NaI)=n(AgNO3)=0.1mol/L×0.019L=0.0019mol,
则3.000g样品中含有n(NaI)=0.019mol,m(NaI)=0.019mol×150g/mol=2.85g,
ω(NaI)=
| 2.85g |
| 3.000g |
故答案为:95.00%;
③若用上述方法测定产品中NaI的质量分数偏低,可考虑样品的原因,两种情况,一是样品被氧化,二是样品吸水,
故答案为:样品在空气中被氧化;样品在空气中吸水.
点评:本题考查物质制备实验,明确制备流程中发生的反应及操作为解答的关键,涉及氧化还原反应及碘的特性,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列各表述与示意图一致的是( )
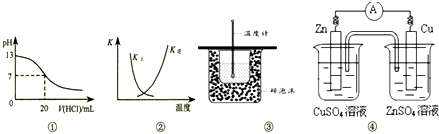

| A、图①表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| B、图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 |
| C、图③装置用于测定中和热 |
| D、图④装置可以构成锌、铜、硫酸铜溶液原电池 |
碳原子的摩尔质量是( )
| A、12 | B、12g/mol |
| C、12mol | D、12g |