题目内容
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、无色溶液:Ca2+、H+、Cl-、HSO3 - | ||
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3 - | ||
| C、Na2CO3溶液:K+、Fe3+、SO42-、NO3 - | ||
D、
|
考点:离子共存问题
专题:离子反应专题
分析:A.反应生成二氧化硫和水;
B.能使pH试纸呈红色的溶液呈酸性;
C.与CO32-反应的离子不能大量共存;
D.
=0.1 mol/L的溶液呈碱性.
B.能使pH试纸呈红色的溶液呈酸性;
C.与CO32-反应的离子不能大量共存;
D.
| Kw |
| C(H+) |
解答:
解:A.H+、HSO3-反应生成二氧化硫和水,不能大量共存,故A错误;
B.能使pH试纸呈红色的溶液呈酸性,酸性条件下,I-、NO3-发生氧化还原对应,不能大量共存,故B错误;
C.Fe3+与CO32-反应的离子不能大量共存,故C错误;
D.
=0.1 mol/L的溶液呈碱性,碱性条件下,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.能使pH试纸呈红色的溶液呈酸性,酸性条件下,I-、NO3-发生氧化还原对应,不能大量共存,故B错误;
C.Fe3+与CO32-反应的离子不能大量共存,故C错误;
D.
| Kw |
| C(H+) |
故选D.
点评:本题考查离子共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意离子的性质以及反应类型的判断,题目难度不大.

练习册系列答案
相关题目
某一有机物A可发生下列变化:已知C为羧酸,且C、E不发生银镜反应,则A的可能结构有( )
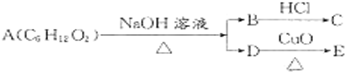
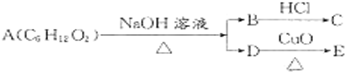
| A、1种 | B、3种 | C、2种 | D、1种 |
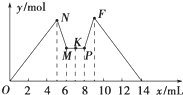 如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )| A、N点时溶液中的溶质只有NaCl |
| B、M点之前加入的是NaOH溶液,M点之后加入的是盐酸 |
| C、c(NaOH)=c(HCl) |
| D、原混合溶液中c(MgCl2):c(AlCl3)=1:1 |
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | Ki=3×10-8 |
| H2CO3 | Ki1=4.3×10-7 |
| Ki2=5.6×10-11 |
| A、c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| B、c(ClO-)>c(HCO3-)>c(OH-)>c(H+) |
| C、c(HCO3-)>c(ClO-)>c(OH-)>c(H+) |
| D、c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
同物质的量浓度、同体积的HCl和醋酸溶液,分别与过量相同情况的Na2CO3固体反应时,下列叙述正确的是( )
| A、反应速率HCl>CH3COOH |
| B、气泡逸出速率CH3COOH>HCl |
| C、在相同条件下两酸产生的CO2的体积不相同 |
| D、如果两酸的c(H+)相同时,两酸的物质的量浓度HCl>CH3COOH |
从利用金属的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序主要跟下列有关的是( )
①地壳中金属元素的含量;
②金属活动性顺序;
③金属的导电性;
④金属冶炼的难易程度.
①地壳中金属元素的含量;
②金属活动性顺序;
③金属的导电性;
④金属冶炼的难易程度.
| A、①③ | B、②④ | C、③⑤ | D、②⑤ |
下列过程属于熵增加的是( )
| A、一定条件下,水由气态变为液态 |
| B、2H2(g)+O2(g)═2H2O(g) |
| C、HCl(g)+NH3(g)═NH4Cl(s) |
| D、NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g) |
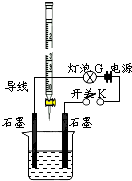 常温下,水的离子积Kw=1×10-14.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.
常温下,水的离子积Kw=1×10-14.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.