题目内容
SO2和NOx都是大气污染物.
(1)直接排放含SO2的烟气会形成酸雨,危害环境.用化学方程式表示SO2形成硫酸型酸雨的过程 .
(2)表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量.请你分析雨后或风速较大时SO2平均含量较低的原因:
①雨后: ;②风俗较大时: .
(3)洗涤含SO2的烟气,以下物质不能作为洗涤剂的是 (填字母序号).
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
FeS2
Fe2++S
Fe3+
①该技术的第一步反应的是离子方程式为
②处理1kg含80%FeS2的黄铁矿,第二部消耗O2(标况)的体积为 L(保留一位小数)
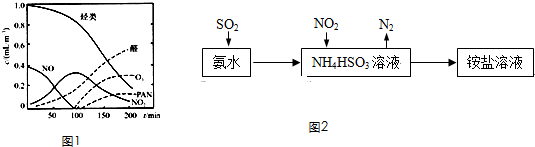
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图1所示.由图可知,光化学烟雾是指等污染物气体和颗粒物所形成的烟雾,则 可以减少光化学烟雾的发生.
(6)氧化-还原法消除NOx的转化如下:
NO
NO2
N2
①反应Ⅰ为NO+O3=NO2+O2,生成11.2L O2(标况)时,转移电子的物质的量是 mol.
②反应Ⅱ中,当n(NO2):n[CO(NH2)2]=3:2时,反应的化学方程式是 .
(7)利用氨气可以将SO2和NO2吸收,原理如图2所示:NO2被吸收的离子方程式是 .
(1)直接排放含SO2的烟气会形成酸雨,危害环境.用化学方程式表示SO2形成硫酸型酸雨的过程
(2)表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量.请你分析雨后或风速较大时SO2平均含量较低的原因:
①雨后:
| 天气情况 | 平均风速(m/s) | 空气中SO2的平均含量(mg/L) |
| 雨前 | 2.0 | 0.03 |
| 雨后 | 2.2 | 0.01 |
| 晴 | 23.0 | 0.015 |
| 晴 | 0.9 | 0.03 |
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
FeS2
| 在微生物的作用下 |
| +O2+H2O |
| O | 2 4 |
| 在微生物作用下 |
| +O2+H+ |
①该技术的第一步反应的是离子方程式为
②处理1kg含80%FeS2的黄铁矿,第二部消耗O2(标况)的体积为
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图1所示.由图可知,光化学烟雾是指等污染物气体和颗粒物所形成的烟雾,则
(6)氧化-还原法消除NOx的转化如下:
NO
| O3 |
| 反应Ⅰ |
| CO(NH2)2 |
| 反应Ⅱ |
①反应Ⅰ为NO+O3=NO2+O2,生成11.2L O2(标况)时,转移电子的物质的量是
②反应Ⅱ中,当n(NO2):n[CO(NH2)2]=3:2时,反应的化学方程式是
(7)利用氨气可以将SO2和NO2吸收,原理如图2所示:NO2被吸收的离子方程式是

考点:二氧化硫的污染及治理,氮的氧化物的性质及其对环境的影响
专题:
分析:(1)二氧化硫与水反应生成亚硫酸,又被氧化为硫酸;
(2)①根据SO2能和水反应;②根据风速越大,气体扩散速度越大;
(3)依据二氧化硫的性质:是一种酸性氧化物可以和碱反应,二氧化硫溶于水得亚硫酸,酸性强于碳酸,所以可以和碳酸钠溶液反应;
(4)①根据反应物结合质量守恒定律、电荷守恒书写离子方程式并判断生成物; ②根据元素守恒和化学方程式进行计算;
(5)依据图象分析可知NO,NO2、烃等在紫外线照射下生成O3、醛、PAN等污染物,从而形成光化学烟雾,而汽车尾气是排放氮氧化物和烃类的主要来源;
(6)①化合价升高值=化合价降低值=转移电子数,根据化合价的变化来确定电子转移数目;
②反应方程式中,系数之比等于物质的量之比;
(7)二氧化氮与水反应生成硝酸,硝酸具有强的氧化性,能够氧化亚硫酸氢根离子.
(2)①根据SO2能和水反应;②根据风速越大,气体扩散速度越大;
(3)依据二氧化硫的性质:是一种酸性氧化物可以和碱反应,二氧化硫溶于水得亚硫酸,酸性强于碳酸,所以可以和碳酸钠溶液反应;
(4)①根据反应物结合质量守恒定律、电荷守恒书写离子方程式并判断生成物; ②根据元素守恒和化学方程式进行计算;
(5)依据图象分析可知NO,NO2、烃等在紫外线照射下生成O3、醛、PAN等污染物,从而形成光化学烟雾,而汽车尾气是排放氮氧化物和烃类的主要来源;
(6)①化合价升高值=化合价降低值=转移电子数,根据化合价的变化来确定电子转移数目;
②反应方程式中,系数之比等于物质的量之比;
(7)二氧化氮与水反应生成硝酸,硝酸具有强的氧化性,能够氧化亚硫酸氢根离子.
解答:
解:(1)二氧化硫与水反应生成亚硫酸,又被氧化为硫酸,则SO2形成硫酸型酸雨的反应为SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4,
故答案为:SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4;
(2)①SO2能和水反应,所以雨后空气中SO2的含量降低,故答案为:可能是下雨时SO2和水反应降低了雨后空气中SO2的含量;
②风速越大,气体扩散速度越大,SO2浓度也就越小,故答案为:风速越大,气体扩散速度越大,空气中SO2浓度越小;
(3)洗涤含SO2的烟气,根据酸性氧化物的性质选a.Ca(OH)2 b.Na2CO3,故答案为:cd;
(4)①第一步反应中反应物有FeS2、O2和H2O,生成物有Fe2+和SO42-,根据氧化还原反应得失电子数目相等,则有2FeS2~7O2,根据电荷守恒,还应有生成H+,则反应的离子方程式为2FeS2+7O2+2H2O=4H++2Fe2++4SO42-,
故答案为:2FeS2+7O2+2H2O=4H++2Fe2++4SO42-;
②1kg含80%FeS2能生成二价铁离子的物质的量是
=6.67mol,
设消耗O2(标况)的体积为X,
4Fe2++O2+4H+=4Fe3++2H2O
4 22.4×2
6.67 X
=
解得,X=74.7L
故答案为:74.7;
(5)依据图象分析可知NO,NO2、烃等在紫外线照射下生成O3、醛、PAN等污染物,从而形成光化学烟雾,而汽车尾气是排放氮氧化物和烃类的主要来源,故减少汽车尾气可以减少光化学烟雾的发生,
故答案为:减少机动车有害气体尾气的排放;
(6)①NO+O3═NO2+O2,生成1mol氧气转移电子是2mol,生成11.2L即0.5mol O2(标准状况)时,转移电子的物质的量是1mol,故答案为:1;
②当n(NO2):n[CO(NH2)2]=3:2,即NO2和CO(NH2)2的系数之比是3:2,其方程式表示为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2,故答案为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2;
(7)二氧化氮与水反应生成硝酸,硝酸具有强的氧化性,能够氧化亚硫酸氢根离子,反应的离子方程式为:2NO2+4HSO3-=N2+4SO42-+4H+,
故答案为:2NO2+4HSO3-=N2+4SO42-+4H+.
故答案为:SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4;
(2)①SO2能和水反应,所以雨后空气中SO2的含量降低,故答案为:可能是下雨时SO2和水反应降低了雨后空气中SO2的含量;
②风速越大,气体扩散速度越大,SO2浓度也就越小,故答案为:风速越大,气体扩散速度越大,空气中SO2浓度越小;
(3)洗涤含SO2的烟气,根据酸性氧化物的性质选a.Ca(OH)2 b.Na2CO3,故答案为:cd;
(4)①第一步反应中反应物有FeS2、O2和H2O,生成物有Fe2+和SO42-,根据氧化还原反应得失电子数目相等,则有2FeS2~7O2,根据电荷守恒,还应有生成H+,则反应的离子方程式为2FeS2+7O2+2H2O=4H++2Fe2++4SO42-,
故答案为:2FeS2+7O2+2H2O=4H++2Fe2++4SO42-;
②1kg含80%FeS2能生成二价铁离子的物质的量是
| 1000×80% |
| 120 |
设消耗O2(标况)的体积为X,
4Fe2++O2+4H+=4Fe3++2H2O
4 22.4×2
6.67 X
| 4 |
| 6.67 |
| 22.4×2 |
| X |
解得,X=74.7L
故答案为:74.7;
(5)依据图象分析可知NO,NO2、烃等在紫外线照射下生成O3、醛、PAN等污染物,从而形成光化学烟雾,而汽车尾气是排放氮氧化物和烃类的主要来源,故减少汽车尾气可以减少光化学烟雾的发生,
故答案为:减少机动车有害气体尾气的排放;
(6)①NO+O3═NO2+O2,生成1mol氧气转移电子是2mol,生成11.2L即0.5mol O2(标准状况)时,转移电子的物质的量是1mol,故答案为:1;
②当n(NO2):n[CO(NH2)2]=3:2,即NO2和CO(NH2)2的系数之比是3:2,其方程式表示为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2,故答案为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2;
(7)二氧化氮与水反应生成硝酸,硝酸具有强的氧化性,能够氧化亚硫酸氢根离子,反应的离子方程式为:2NO2+4HSO3-=N2+4SO42-+4H+,
故答案为:2NO2+4HSO3-=N2+4SO42-+4H+.
点评:本题综合考查了二氧化硫含量的测定以及二氧化硫的来源与危害、化学平衡图象,化学平衡影响因素及有关计算、电化学和热化学的综合知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该有机物属于烃 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定不含有氧元素 |
两种金属组成的合金5.6g,与氯气完全反应,消耗氯气7.1g,则合金的组成可能( )
| A、Cu和Zn |
| B、Al和Zn |
| C、Al 和 Na |
| D、Cu和Fe |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、无色溶液:Ca2+、H+、Cl-、HSO3 - | ||
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3 - | ||
| C、Na2CO3溶液:K+、Fe3+、SO42-、NO3 - | ||
D、
|
下列有关电解质溶液中粒子浓度关系正确的是( )
| A、pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| B、含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C、常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<③<② |
| D、NaHCO3溶液中:c(Na+)>c( HCO3-)>c(OH-)>c(H+)>c(CO32-) |
工业制硝酸的其中一步反应为氨的氧化,反应方程式为:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol氧化过程中还伴随有N2O、N2等物质生成.有关该反应的说法正确的是( )
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol氧化过程中还伴随有N2O、N2等物质生成.有关该反应的说法正确的是( )
| A、此反应物的总能量低于生成物的总能量 |
| B、反应达到平衡后,3ν正(NH3)=2ν逆(H2O) |
| C、其它条件不变,温度越高,氨的转化率越高 |
| D、寻找合适的催化剂是加快反应速率的有效措施 |
在四个不同的容器中,在不同条件下进行合成氨的反应,根据下列在相同时间内测定的结果判断生成氨的速率最快的是( )
| A、v(H2)=0.1 mol/(L?min) |
| B、v(N2)=0.1 mol/(L?min) |
| C、v(N2)=0.2 mol/(L?min) |
| D、v(NH3)=0.3 mol/(L?min) |