题目内容
8.下列化学反应中,属于吸热反应的是( )| A. | 木炭燃烧反应 | B. | 稀硫酸与烧碱反应 | ||
| C. | 生石灰与水反应 | D. | Ba(OH)2•8H2O与NH4Cl晶体 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A.木炭燃烧反应是放热反应,故A错误;
B.稀硫酸与烧碱反应属于中和反应,反应为放热反应,故B错误;
C.生石灰变成熟石灰的反应是放热反应,故C错误;
D.Ba(OH)2•8H2O与NH4Cl晶体混合反应是吸热反应,在反应中吸收热量,故D正确;
故选D.
点评 本题考查化学反应的热量变化,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18. 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
(1)一定温度下,反应2NO2(g)?N2O4 (g)△S<0,该反应能自发进行的原因是△H<0(选填“=”、“>”、“<”)
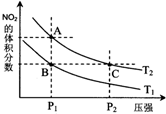
(2)对反应2NO2(g)?N2O4(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是D
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
(3)在100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为0.0025mol•(L•s)-1.
②2NO2(g)?N2O4(g)该反应的平衡常数K的值为2.8;若100℃时的某时刻测得c(NO2)=1.00mol/L,c(N2O4)=0.20mol/L,则该时刻的v正>v逆(填“>”、“<”或“=”),升高温度后,反应2NO2?N2O4的平衡常数K将减小(填“增大”、“减小”或“不变”).
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是0.10mol•L-1.
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.(1)一定温度下,反应2NO2(g)?N2O4 (g)△S<0,该反应能自发进行的原因是△H<0(选填“=”、“>”、“<”)
(2)对反应2NO2(g)?N2O4(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是D
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
(3)在100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②2NO2(g)?N2O4(g)该反应的平衡常数K的值为2.8;若100℃时的某时刻测得c(NO2)=1.00mol/L,c(N2O4)=0.20mol/L,则该时刻的v正>v逆(填“>”、“<”或“=”),升高温度后,反应2NO2?N2O4的平衡常数K将减小(填“增大”、“减小”或“不变”).
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是0.10mol•L-1.
19.五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请按要求回答下列问题:
(1)X元素名称碳,W的离子结构示意图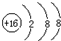 ;
;
(2)元素Z位于周期表中的位置是第三周期第VA族;
(3)元素Z可以形成多种单质,请任意写出一种常见单质的名称白磷或红磷;
(4)Y的最高价氧化物的化学式为N2O5;M的最高价氧化物水化物名称为高氯酸;
(5)Z、W、M三种元素中,原子半径最大的是P(填元素符号);这三者与氢元素形成的化合物中,最稳定的是HCl(填:氢化物的化学式),它的电子式为 ;
;
(6)X与M可形成XM4型化合物,是一种常见的溶剂,其中的化学键类型是共价键(填:“离子键”或“共价键”)
(7)W的氧化物有两种A和B,已知在某一定条件下,A和B能同时相互转化.则在该条件下A不能完全转化为B(填:“能”或“不能”)
| X | Y | ||
| Z | W | M |
(1)X元素名称碳,W的离子结构示意图
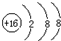 ;
;(2)元素Z位于周期表中的位置是第三周期第VA族;
(3)元素Z可以形成多种单质,请任意写出一种常见单质的名称白磷或红磷;
(4)Y的最高价氧化物的化学式为N2O5;M的最高价氧化物水化物名称为高氯酸;
(5)Z、W、M三种元素中,原子半径最大的是P(填元素符号);这三者与氢元素形成的化合物中,最稳定的是HCl(填:氢化物的化学式),它的电子式为
 ;
;(6)X与M可形成XM4型化合物,是一种常见的溶剂,其中的化学键类型是共价键(填:“离子键”或“共价键”)
(7)W的氧化物有两种A和B,已知在某一定条件下,A和B能同时相互转化.则在该条件下A不能完全转化为B(填:“能”或“不能”)
16.Ⅰ.高炉炼铁是冶炼铁的主要方法,发生的主要反应为
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为60%.
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.
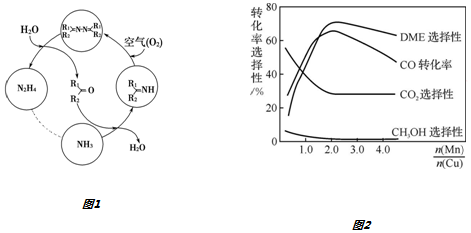
Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.

Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
3.等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液完全反应后,溶液中有关离子浓度之间不存在的关系是( )
| A. | c(H+)•c(OH-)=KW | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)+c(OH-) | D. | c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
20.下列各组离子中,在给定条件下能够大量共存的是( )
| A. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| B. | 无色溶液中:Mg2+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- |
17.下列烷烃分子中,一氯取代产物最多的是( )
| A. | 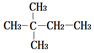 | B. | 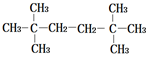 | ||
| C. | CH3CH2CH2CH2CH2CH3 | D. | CH3CH2CH2CH2CH2CH2CH3 |
18.下列各组物质中,互为同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 淀粉和纤维素 | C. | 核糖和脱氧核糖 | D. | 丙氨酸、甘氨酸 |