题目内容
18.下列各组物质中,互为同分异构体的是( )| A. | 葡萄糖和果糖 | B. | 淀粉和纤维素 | C. | 核糖和脱氧核糖 | D. | 丙氨酸、甘氨酸 |
分析 分子式相同、结构不同的化合物之间互为同分异构体,结合有机物的分子组成、结构特点进行判断.
解答 解:A.果糖、葡萄糖分子式相同、结构不同,二者互为同分异构体,故A正确;
B.淀粉和纤维素是多糖,高分子化合物,化学式中的n值不同,不是同分异构体,故B错误;
C.核糖分子比脱氧核糖分子多1个O原子,二者分子式不同,不属于同分异构体,故C错误;
D.甘氨酸结构简式为H2NCH2COOH;丙氨酸的结构简式为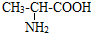 ,二者含有C原子数不同,则分子式不同,二者不属于同分异构体,故D错误;
,二者含有C原子数不同,则分子式不同,二者不属于同分异构体,故D错误;
故选A.
点评 本题考查了同分异构体的判断,题目难度不大,明确同分异构体的概念及判断方法为解答关键,试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
8.下列化学反应中,属于吸热反应的是( )
| A. | 木炭燃烧反应 | B. | 稀硫酸与烧碱反应 | ||
| C. | 生石灰与水反应 | D. | Ba(OH)2•8H2O与NH4Cl晶体 |
9.下列各溶液中一定能大量共存的离子组是( )
| A. | 使酚酞试液呈红色的溶液中:K+、Na+、SO42-、NO3- | |
| B. | 使pH试纸呈红色的溶液中:Fe3+、Na+、SCN-、Cl- | |
| C. | 0.1mol/LNaHCO3溶液中:K+、AlO2-、SO42-、NO3- | |
| D. | 加入Al粉能产生H2的溶液中:K+、Na+、AlO2-、CO32- |
6.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+K+ SO42- HCO3- | B. | Cu2+ K+ SO42- NO3- | ||
| C. | Na+ K+ Cl- NO3- | D. | Al3+ K+ SO42-OH- |
13.在100mL2mol/L的盐酸反应中分别加入等物质的量的金属Na、Mg、Al,充分生成气体的体积均为VL(标准状况下),下列说法正确的是( )
| A. | 反应中,每生成1molH2转移的电子数均为2mol | |
| B. | 参加反应的金属Na、Mg、Al的物质的量之比为1:2:3 | |
| C. | 镁的物质的量为0.1mol | |
| D. | V=2.24 |
3.下列离子方程式中,正确的是( )
| A. | 盐酸滴在大理石上:2H++CO32-═CO2↑+H2O | |
| B. | 硫酸滴在钢片上:Cu+2H+═Cu2++H2↑ | |
| C. | 向NaOH溶液中通入过量CO2:OH-+CO2═HCO3- | |
| D. | 氢氧化铜与稀硫酸反应:H++OH-═H2O |
7.不能用金属单质与非金属单质直接化合而得到的物质是( )
| A. | FeCl3 | B. | FeCl2 | C. | Fe3O4 | D. | CuCl2 |
16.甲醇是重要的化工原料.利用合成气(主要成分CO,CO2和H2)在催化剂的作用下合成甲醇,发生主要反应如下:
?CO(g)+2H2(g)?CH3OH(g)?CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
甲醇与CO的结构式分别如图:
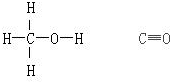
(1)已知反应?中相关化学键键能数据如表:
利用反应?合成1mol甲醇反应放出(填“放出”或“吸收”)能量99kJ
(2)温度为110℃条件下,向体积2L的密闭容器充2molCO2与4molH2,发生反应?,10min后达到平衡状态后测得甲醇浓度为0.5mol.L-1.求氢气的反应速率:0.15mol/(L•min).
(3)将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题: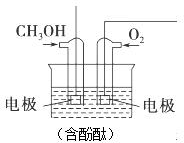
通入甲醇的电极是负(填“正”或“负”)极,反应时该电极附近的现象是溶液红色变浅,溶液中K+向正(填“正”或“负”)极移动:写出正极反应式:O2+2H2O+4e-=4OH-;若电池工作过程中通过2mol电子,则理论上消耗O211.2L(标准状况).
?CO(g)+2H2(g)?CH3OH(g)?CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
甲醇与CO的结构式分别如图:
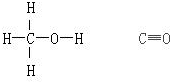
(1)已知反应?中相关化学键键能数据如表:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| 键能(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)温度为110℃条件下,向体积2L的密闭容器充2molCO2与4molH2,发生反应?,10min后达到平衡状态后测得甲醇浓度为0.5mol.L-1.求氢气的反应速率:0.15mol/(L•min).
(3)将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:

通入甲醇的电极是负(填“正”或“负”)极,反应时该电极附近的现象是溶液红色变浅,溶液中K+向正(填“正”或“负”)极移动:写出正极反应式:O2+2H2O+4e-=4OH-;若电池工作过程中通过2mol电子,则理论上消耗O211.2L(标准状况).