题目内容
硫酸的浓度为0.005mol/L,则溶液的PH值为( )
| A、2 | B、4 | C、10 | D、12 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:硫酸为强电解质,在水中能够完全电离,根据氢离子浓度和硫酸浓度的关系结合pH=-lgc(H+)计算;
解答:
解:硫酸为强电解质,在水中能够完全电离,电离方程式为:H2SO4=2H++SO42-,c(H+)=2c(H2SO4)=2×0.005mol/L=0.01mol/L,
pH=-lgc(H+)=2,
故选A.
pH=-lgc(H+)=2,
故选A.
点评:本题考查了PH的简单计算,注意硫酸为二元强酸,氢离子浓度为硫酸浓度的两倍为解答的关键,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、油脂是高级脂肪酸的甘油酯 |
| B、油脂有油和脂肪之分,但都属于酯 |
| C、油脂水解可得到氨基酸和甘油 |
| D、油脂不能使溴水褪色 |
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
| A、硝酸为弱电解质 |
| B、该溶液1 mL稀释至100 mL后,pH小于3 |
| C、向该溶液中加入等体积、等浓度的氢氧化钡溶液,混合后溶液pH=7 |
| D、该溶液中水电离出的c(H+)=1×10-13 mol/L |
一定温度下,可逆反应2NO2?2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③混合气体的平均相对分子质量不再改变的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态.
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③混合气体的平均相对分子质量不再改变的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态.
| A、①③④ | B、①④⑥ |
| C、②③⑤ | D、①②③④⑤⑥ |
下列说法正确的是( )
| A、光导纤维的主要成分是硅,可广泛用于通信和医疗领域 |
| B、水晶和金刚石都是由碳元素组成的宝石 |
| C、氮化硅、光导纤维等属于新型无机非金属材料 |
| D、合金的熔点一般比组成合金的各成分金属高 |
下列有机化合物中不属于烃的是( )
| A、乙烷 | B、乙烯 | C、乙醇 | D、苯 |
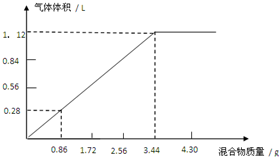 在硝酸铵和硫酸铵的固体混合物中加入50mL NaOH溶液,充分加热反应,混合的质量与产生的气体的体积如图所示.
在硝酸铵和硫酸铵的固体混合物中加入50mL NaOH溶液,充分加热反应,混合的质量与产生的气体的体积如图所示.