题目内容
已知某饱和 NaCl 溶液的体积为V mL.密度为ρ g/cm3,质量分数为 w%.物质的量浓度为c mol/L,溶液中含NaCl的质量为m g.
(1)用m、V表示溶液物质的量浓度 .
(2)用w、ρ表示溶液物质的量浓度 .
(3)用c、ρ表示溶液的质量分数 .
(4)用w表示该温度下NaCl的溶解度 .
(1)用m、V表示溶液物质的量浓度
(2)用w、ρ表示溶液物质的量浓度
(3)用c、ρ表示溶液的质量分数
(4)用w表示该温度下NaCl的溶解度
考点:物质的量浓度的相关计算,溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:(1)根据n=
计算氯化钠物质的量,再根据c=
计算;
(2)根据c=
计算;
(3)根据c=
进行公式变形计算;
(4)饱和溶液的质量分数w=
,据此计算溶解度.
| m |
| M |
| n |
| V |
(2)根据c=
| 1000ρω |
| M |
(3)根据c=
| 1000ρω |
| M |
(4)饱和溶液的质量分数w=
| s |
| 100+s |
解答:
解:(1)mg氯化钠物质的量=
=
mol,溶液体积为VmL,则溶液物质的量浓度=
=
mol/L,故答案为:
mol/L;
(2)根据c=
可知,溶液物质的量浓度=
mol/L=
mol/L,故答案为:
mol/L;
(3)根据c=
可知,w%=
=
%,故答案为:
%;
进行公式变形计算;
(4)令溶解度为s,该饱和溶液的质量分数w%=
,解得s=
g,故答案为:
g.
| mg |
| 58.5g/mol |
| m |
| 58.5 |
| ||
| V×10-3L |
| 1000m |
| 58.5V |
| 1000m |
| 58.5V |
(2)根据c=
| 1000ρω |
| M |
| 1000×ρ×w% |
| 58.5 |
| 10ρw |
| 58.5 |
| 10ρw |
| 58.5 |
(3)根据c=
| 1000ρω |
| M |
| 58.5c |
| 1000ρ |
| 58.5c |
| 10ρ |
| 58.5c |
| 10ρ |
进行公式变形计算;
(4)令溶解度为s,该饱和溶液的质量分数w%=
| s |
| 100g+s |
| 100w |
| 100-w |
| 100w |
| 100-w |
点评:本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数、溶解度,难度不大,注意对公式的理解与灵活应用,理解掌握物质的量浓度与质量分数之间的关系.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
2012年4月,中央电视台曝光了不法商贩将重金属铬(Cr)超标的工业明胶加工成药用胶囊的“毒胶囊”事件.已知铬的原子序数为24,下列叙述正确的是( )
| A、铬位于元素周期表的第四周期第Ⅷ族 | ||
B、中子数为29的铬原子符号表示为
| ||
| C、已知铬元素的一种同位素的质量数为53,则该同位素有53个中子 | ||
| D、警察通过装有橙色的酸性重铬酸钾的装置检查司机是否酒后驾车 |
下列各项表达中正确的是( )
A、Na2O2的电子式为 |
| B、二氧化硅的分子式为SiO2 |
C、氦原子的电子排布图为  |
D、Cl-的结构示意图为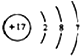 |
下列关于化学键的叙述不正确的是( )
| A、离子化合物一定含有离子键 |
| B、共价键只存在于共价化合物中 |
| C、化学键的形成与成键原子结构有关,主要通过原子之间价电子的得失或共用来实现 |
| D、化学反应的本质是旧键断裂,新键形成 |
 在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题:
在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题: