题目内容
 化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染.电化学降解NO3-的原理如图所示.
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染.电化学降解NO3-的原理如图所示.电源正极为
考点:电解原理
专题:电化学专题
分析:根据图象知,硝酸根离子得电子发生氧化反应,则Ag-Pt作阴极,Pt电极为阳极,A为正极,B为负极,以此解答该题.
解答:
解:由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A;2NO3-+10e-+12H+=6H2O+N2↑.
故答案为:A;2NO3-+10e-+12H+=6H2O+N2↑.
点评:本题考查了电解原理,明确阴阳极上发生的电极反应及离子移动方向、阴阳极的判断方法等知识点即可解答,难点是电极反应式的书写,难度中等.

练习册系列答案
相关题目
如图实验装置或操作能达到目的是( )
A、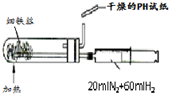 合成氨并检验氨的生成 |
B、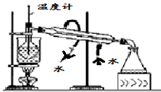 碘的CCl4溶液中分离I2并回收CCl4 |
C、 分离CH3CH2OH和CH3COOC2H5混合液 |
D、 制备Fe(OH)2 |
下列表示对应化学反应的离子方程式正确的是( )
| A、Na2CO3溶液的水解:CO32-+H3O+?HCO3-+H2O |
| B、钢铁吸氧腐蚀时,负极反应式为:4OH--4e-═2H2O+O2↑ |
| C、向Al2(SO4)3溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀:2Al3++3SO42-+8OH-+3Ba2+═2AlO2-+3BaSO4↓+4H2O |
| D、氯化亚铁溶液中滴入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |



 )在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式:
)在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式:
 石棉矿是天然纤维状硅酸盐类矿物的总称,可分为蛇纹石石棉矿(又称温石棉矿)和闪石类石棉矿两大类.蛇纹石石棉矿具有优良的性能,在工业中应用广泛,在国防和航天工业中亦有许多用途.
石棉矿是天然纤维状硅酸盐类矿物的总称,可分为蛇纹石石棉矿(又称温石棉矿)和闪石类石棉矿两大类.蛇纹石石棉矿具有优良的性能,在工业中应用广泛,在国防和航天工业中亦有许多用途.