题目内容
用石墨做电极电解下列溶液,电解完成后,向剩余的溶液中加入适量蒸馏水,能使溶液和电解前相同的是( )
| A、NaCl |
| B、Na2SO4 |
| C、HCl溶液 |
| D、AgNO3 |
考点:电解原理
专题:电化学专题
分析:电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同,应为电解水型的电解,电解时阳极反应为:4OH--4e-=2H2O+O2↑,阴极反应为:4H++4e-=2H2↑,可为电解含氧酸溶液、强碱溶液或活泼金属的含氧酸盐溶液,以此解答该题.
解答:
解:A.电解NaCl,生成NaOH、H2、Cl2,加盐酸显然不能恢复电解前的状态,应通入适量的HCl气体,故A错误.
B.电解Na2SO4,阳极生成氧气,阴极生成氢气,实际为电解水,电解后加入水可恢复到原来的浓度,故B正确;
C.电解HCl,阳极生成氯气,阴极生成氢气,实际为电解本身,电解后加入水不可恢复到原来的浓度,故C错误;
D.电解AgNO3,阳极析出Ag,阴极生成O2,要使溶液恢复到原来的浓度,应加入Ag2O,故D错误;
故选B.
B.电解Na2SO4,阳极生成氧气,阴极生成氢气,实际为电解水,电解后加入水可恢复到原来的浓度,故B正确;
C.电解HCl,阳极生成氯气,阴极生成氢气,实际为电解本身,电解后加入水不可恢复到原来的浓度,故C错误;
D.电解AgNO3,阳极析出Ag,阴极生成O2,要使溶液恢复到原来的浓度,应加入Ag2O,故D错误;
故选B.
点评:本题考查电解原理,侧重于电解水型的考查,题目难度不大,注意阴阳离子的放电顺序,把握电解特点和规律.

练习册系列答案
相关题目
下列叙述不能达到电镀目的是( )
| A、铜作阳极,锌作阴极,硫酸铜作电解质溶液 |
| B、锌作阳极,铜作阴极,硫酸锌作电解质溶液 |
| C、铁接在直流电源的正极,银接在直流电源的负极,硝酸银溶液作电解质溶液 |
| D、铁接在直流电源的负极,银接在支流电源的正极,硝酸银溶液作电解质溶液 |
(双项)下列说法正确的是( )
| A、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、电解水时为增强导电性可以加入少量的CuCl2固体 |
| C、电解精炼粗铜时,金、银等活泼性较弱的金属在阳极沉积成阳极泥 |
| D、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
用石墨电极电解CuSO4和KNO3的混合溶液500mL,经一段时间电解后,两极都得到11.2L气体(标准状况下体积),则此混合液中硫酸铜的物质的量浓度为( )
| A、0.5mol/L |
| B、1mol/L |
| C、0.8mol/L |
| D、1.5mol/L |
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答: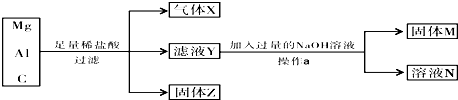
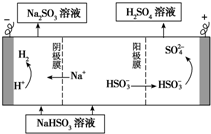 工业生产中用SO2为原料制取硫酸
工业生产中用SO2为原料制取硫酸