题目内容
8.已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol,下列说法正确的是( )| A. | 2 L二氧化碳分解生成2 L一氧化碳和1 L氧气吸收576 kJ热量 | |
| B. | 恒压条件下生成物的总焓大于反应物的总焓 | |
| C. | 在相同条件下,2 mol一氧化碳与1 mol氧气的能量总和大于2 mol二氧化碳的能量 | |
| D. | 一氧化碳的燃烧热是566 kJ/mol |
分析 热化学方程式中化学计量数表示物质的量,且物质的量与热量成正比,反应遵循能量守恒定律,燃烧热为1molCO燃烧放出的热量,以此来解答.
解答 解:A.化学计量数不能表示体积关系,且状况未知,不能确定体积与热量的关系,故A错误;
B.反应遵循能量守恒,该反应为放热反应,放热反应中生成物的总焓小于反应物的总焓,故B错误;
C.该反应为放热反应,放热反应中反应物的总能量大于生成物的总能量,则在相同条件下,2 mol一氧化碳与1 mol氧气的能量总和大于2 mol二氧化碳的能量,故C正确;
D.由2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol可知,1molCO燃烧放出热量为283kJ,则一氧化碳的燃烧热是283 kJ/mol,故D错误;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、热化学方程式中的化学计量数、燃烧热为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列有关厨房铝制品的使用中,你认为合理的是( )
| A. | 盛放食醋 | B. | 烧煮开水 | C. | 盛放咸的食物 | D. | 用碱水洗涤 |
13.某研究性学习小组设计实验用30mL浓硫酸与10mL无水乙醇共热制备乙烯气体、并测定乙醇转化成乙烯的转化率.已知生成的乙烯气体中含有SO2、CO2、乙醇和乙醚等杂质.有关数据如表:
(1)制备乙烯
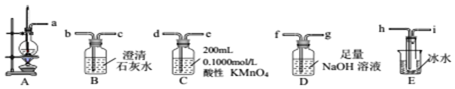
①从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为a→h、i→f、g→d(填仪器接口的字母编号).
②D装置中发生反应的离子方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O实验后,检验D溶液中含有CO32-的实验方案为取少许D溶液于试管中,先滴加足量的双氧水,然后再加入一定量的硫酸,产生能使澄清石灰水浑浊的气体,则证明D溶液中含有CO32-.
③E装置的主要作用是冷凝并收集乙醚.
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4.
已知:C2H4$→_{H+}^{KMnO_{4}}$CO2+H2O;C2O42- $→_{H+}^{KMnO_{4}}$CO2+H2O;MnO4-→Mn2+
④以下情况使得测定乙烯的量偏高的是CD
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤油定终点的现象为溶液由粉红色变成无色,且半分钟内不变色.
⑥已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为2.94%.
| 熔点/℃ | 沸点/℃ | 溶解性 | 颜色状态 | 密度g/cm3 | |
| 乙醇 | -114.1 | 78.3 | 与水、有机溶剂互溶 | 无色液体 | 0.79 |
| 乙醚 | -116.2 | 34.5 | 不溶于水,易溶于有机溶剂 | 无色液体 | 0.7135 |

①从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为a→h、i→f、g→d(填仪器接口的字母编号).
②D装置中发生反应的离子方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O实验后,检验D溶液中含有CO32-的实验方案为取少许D溶液于试管中,先滴加足量的双氧水,然后再加入一定量的硫酸,产生能使澄清石灰水浑浊的气体,则证明D溶液中含有CO32-.
③E装置的主要作用是冷凝并收集乙醚.
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4.
已知:C2H4$→_{H+}^{KMnO_{4}}$CO2+H2O;C2O42- $→_{H+}^{KMnO_{4}}$CO2+H2O;MnO4-→Mn2+
④以下情况使得测定乙烯的量偏高的是CD
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤油定终点的现象为溶液由粉红色变成无色,且半分钟内不变色.
⑥已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为2.94%.
20. 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )| A. | 非金属性:X<T<Z | B. | 第一电离能:X<T<Z | ||
| C. | 气态氢化物的还原性:X<T<R | D. | 最高价氧化物的水化物酸性:Q<T<R |
17.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是( )
| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有 SO42- |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有 I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有 CO32- |
| D | 加入硝酸银 | 产生白色沉淀 | 一定有 Cl- |
| A. | A | B. | B | C. | C | D. | D |
18.用下列实验装置进行相应实验,能达到实验目的是( )
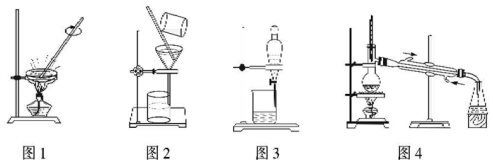

| A. | 用图1所示装置蒸发FeCl3溶液制得无水FeCl3 | |
| B. | 用图2所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 | |
| C. | 用图3所示装置从CH3OH与C2H5OH的混合物中分离出乙醇 | |
| D. | 用图4所示装置从CH3COOH与CH3COOC2H5的混合物中分离出乙酸乙酯 |
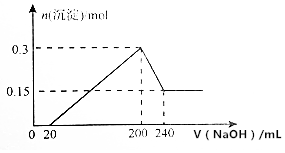 将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示(不考虑金属和盐酸反应时HCl的挥发).
将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示(不考虑金属和盐酸反应时HCl的挥发).