题目内容
14.25℃时,对下列各溶液的叙述中正确的是( )| A. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 4种pH相同的溶液:①CH3COONa ②C6H5ONa ③NaHCO3 ④NaOH,各溶液的物质的量浓度由大到小的顺序是③>②>①>④ | |
| C. | 0.1 mol•L-1HA(某酸)的pH=3,0.1 mol•L-1 BOH(某碱)的pH=13,则BA(盐)溶液的pH<7 | |
| D. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 |
分析 A.醋酸为弱酸,混合液中醋酸过量,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒判断;
B.氢氧化钠是强碱,pH相同时其浓度最小,碳酸氢钠、苯酚钠和醋酸钠都是强碱弱酸盐,盐溶液的碱性强弱取决于阴离子的水解能力,当pH相同时,越难水解的盐,其浓度越大;
C.0.1 mol•L-1HA(某酸)的pH=3,说明HA为弱酸,0.1 mol•L-1 BOH(某碱)的pH=13,说明BOH为强碱,则BA为强碱弱酸盐,溶液呈碱性;
D.根据pH=-lgc(H+)计算氢离子浓度.
解答 解:A.pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,醋酸过量,混合液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故A正确;
B.NaOH为强碱,pH相同时其浓度最小;已知酸性:CH3COOH>H2CO3>C6H5OH,所以水解程度:C6H5ONa>NaHCO3>CH3COONa,当pH相同时,越难水解的盐,其浓度越大,所以浓度大小为:①>③>②>④,故B错误;
C.0.1 mol•L-1HA(某酸)的pH=3,说明HA在溶液中部分电离,为弱酸;0.1 mol•L-1 BOH(某碱)的pH=13,说明BOH在溶液中完全电离,为强碱,则BA(盐)为强碱弱酸盐,其溶液呈碱性,溶液的pH>7,故C错误;
D.pH=2的盐酸溶液中c(H+)=0.01mol/L,pH=l的硫酸溶液中c(H+)=0.1mol/L,二者c(H+)之比为1:10,故D错误;
故选A.
点评 本题考查溶液酸碱性与溶液pH的关系、离子浓度大小比较等知识,题目难度中等,明确溶液酸碱性与溶液pH的关系及计算方法为解答关键,注意掌握盐的水解原理、电荷守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

| A. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 氢氧化钡跟硫酸铜溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 石灰石跟盐酸反应:CO32-+2H+═H2O+CO2↑ |
| A. | NA个H+的质量为1 g | |
| B. | 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+ | |
| C. | 32 g O2中含有2NA个氧原子 | |
| D. | 标准状况下,1 mol H2O中含有NA个分子 |
| A. | Y的转化率为60% | B. | 反应速率v(Y)=0.3 mol/(L•min) | ||
| C. | a的值为2 | D. | 平衡时X的浓度为0.2 mol/L |
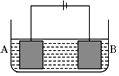 按如图所示的装置进行电解实验.A极是铜镍合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量).通电一段时间后,A极恰好全部溶解,此时B极质量增加3.2g,溶液质量增加0.05g,(已知氧化性,Cu2+>Ni2+)则A合金中铜、镍原子个数比为( )
按如图所示的装置进行电解实验.A极是铜镍合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量).通电一段时间后,A极恰好全部溶解,此时B极质量增加3.2g,溶液质量增加0.05g,(已知氧化性,Cu2+>Ni2+)则A合金中铜、镍原子个数比为( )| A. | 4:1 | B. | 3:1 | C. | 2:1 | D. | 1:1 |
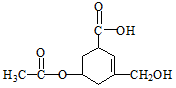
| A. | R的所有原子一定在同一平面上 | |
| B. | 在Ni催化和加热条件下,lmolR能与3molH2发生加成反应 | |
| C. | R既能与羧酸、醇反应,还能发生水解、加成和氧化反应 | |
| D. | 1molR与足量碳酸氢钠溶液反应,生成CO2的物质的量为2mol |
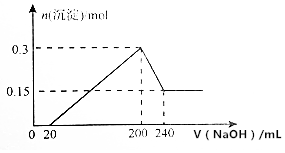 将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示(不考虑金属和盐酸反应时HCl的挥发).
将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示(不考虑金属和盐酸反应时HCl的挥发).