题目内容
11.等质量下列物质与足量稀硝酸反应,放出NO物质的量最多的是( )| A. | Fe2O3 | B. | FeSO4 | C. | Cu | D. | CuO |
分析 假设物质的量质量为1g,计算各物质相应的物质的量,再计算失去电子的物质的量,根据电子转移守恒,可知失去电子越多放出NO物质的量越多.
解答 解:假设物质的量质量为1g,
A.Fe2O3与硝酸不发生氧化还原反应,没有NO生成;
B.FeSO4与硝酸反应被氧化生成Fe3+,则失电子物质的量为$\frac{1}{152}$mol;
C.Cu与硝酸反应生成Cu2+,则失电子物质的量为$\frac{1}{64}$mol×2=$\frac{1}{32}$mol;
D.CuO与不发生氧化还原反应,没有NO生成;
由以上分析可知,失电子最多的是Cu,则放出NO物质的量最多的是Cu,
故选C.
点评 本题考查氧化还原反应的相关计算,侧重于学生的分析能力和计算能力的考查,关键是明确发生的反应,理解掌握氧化还原反应中电子转移守恒应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.在高温下,碘是紫红色蒸气,氢气、碘化氢是无色气体,在某容器中H2+I2?2HI+Q(高温)可逆反应达到平衡,请填写完整表.
| 改变条件 | 平衡移动方向 | 体系内混合气体的颜色变化 |
| (1)加入氢气 | 正反应方向 | 变浅 |
| (2)升高温度 | 逆反应方向 | 变深 |
| (3)加入碘 | 正反应方向 | 变深 |
| (4)使容器的容积压缩到原来的一半 | 不移动 | 变深 |
2.某课外活动小组的同学进行探究银氨溶液温度对丙醛的银镜反应生成速率的影响.实验操作步骤简述如下:
1.准备好实验药品;2.准备好实验仪器;3.配制银氨溶液;4.进行银氨溶液温度对丙醛的银镜反应生成速率的影响探究实验.
请回答下列问题:
(1)丙醛发生银镜反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OHCH3CH2COONH4+2Ag↓+3NH3+H2O.
(2)银镜反应选择的加热方法是乙(填下列装置编号).
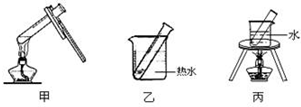
(3)该兴趣小组的同学探究银氨溶液的温度对丙醛的银镜反应生成速率的影响.参照下表格,在实验前拟定好实验记录表格,完整体现实验方案(只列出需记录物理量和单位,不用填写实验数据):
(4)实验完清洗试管内壁附着的银镜方法是:先用稀HNO3溶解,然后再用水清洗
(5)你认为探究丙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的光亮程度.
1.准备好实验药品;2.准备好实验仪器;3.配制银氨溶液;4.进行银氨溶液温度对丙醛的银镜反应生成速率的影响探究实验.
请回答下列问题:
(1)丙醛发生银镜反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OHCH3CH2COONH4+2Ag↓+3NH3+H2O.
(2)银镜反应选择的加热方法是乙(填下列装置编号).

(3)该兴趣小组的同学探究银氨溶液的温度对丙醛的银镜反应生成速率的影响.参照下表格,在实验前拟定好实验记录表格,完整体现实验方案(只列出需记录物理量和单位,不用填写实验数据):
| 实验变量 实验序号 | 银氨溶液的量/mL | |||
| 1 | ||||
| 2 |
(5)你认为探究丙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的光亮程度.
9.根据下列操作及现象,所得结论正确的是( )
| 序号 | 操作及现象 | 结 论 |
| A | 将0.1mol•L-1 Na2CO3溶液稀释到0.01mol•L-1,测得pH变小 | 稀释后CO32-的水解程度减小 |
| B | 向某无色溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 向溴水中加入少量苯,振荡静置后水层为无色 | 苯与Br2发生了加成反应 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有机物相关描述不正确的( )
| A. | 合成顺丁橡胶(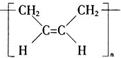 )的单体是CH2=CH-CH=CH2 )的单体是CH2=CH-CH=CH2 | |
| B. | 甲醇、乙二醇、丙三醇都为饱和醇,熔沸点依次递增 | |
| C. | 1mol 绿原酸  通过消去反应脱去1 molH2O时,能得到6 种不同产物(不考虑立体异构) 通过消去反应脱去1 molH2O时,能得到6 种不同产物(不考虑立体异构) | |
| D. | 0.1 mol的 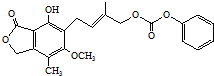 最多能与含0.5 molNaOH的水溶液完全反应 最多能与含0.5 molNaOH的水溶液完全反应 |
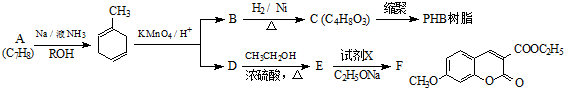
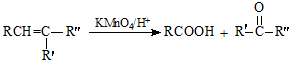
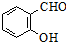 +
+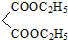 $\stackrel{C_{2}H_{5}ONa}{→}$
$\stackrel{C_{2}H_{5}ONa}{→}$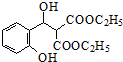 $\stackrel{△}{→}$
$\stackrel{△}{→}$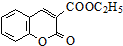
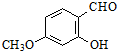 .
.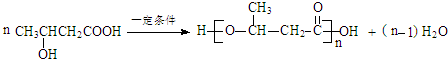 .
. .
.