题目内容
11.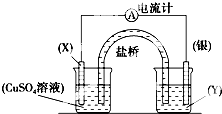 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:(1)电解质溶液Y是AgNO3溶液;
(2)X电极上发生的电极反应为Cu-2e-═Cu2+;
(3)外电路中的电子是从铜电极流向银电极.(填电极材料名称)
分析 含有盐桥的原电池中,电极材料和相对应电解质溶液中阳离子元素相同,原电池放电时,电子从负极沿导线流向正极,负极上失电子发生氧化反应,正极上得电子发生还原反应.
解答 解:(1)含有盐桥的原电池中,电极材料和相对应电解质溶液中阳离子元素相同,所以Y为AgNO3溶液,故答案为:AgNO3溶液;
(2)该原电池中,铜易失电子而作负极,所以电极反应式为:Cu-2e-═Cu2+,故答案为:Cu-2e-═Cu2+;
(3)原电池中电子从负极流向正极,所以从负析铜流向正极银,故答案为:铜;银.
点评 本题考查了原电池原理,明确含有盐桥的原电池中电极材料与相当应电解质溶液中阳离子的关系是解本题关键,注意电子不进入电解质溶液,电解质溶液是通过离子的定向移动形成电流,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.以下物质是按一定规律排列的,Mn、S、MnO2、SO2、K2MnO4、 ,则方框内的物质为( )
,则方框内的物质为( )
 ,则方框内的物质为( )
,则方框内的物质为( )| A. | H2S | B. | Na2SO3 | C. | CuSO4 | D. | Cu2S |
6.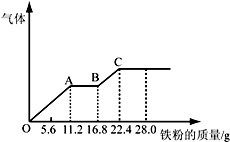 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 混合酸中NO3-物质的量为0.2mol | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | H2SO4浓度为4mol•L-1 |
16.下列化学用语表述正确的是( )
| A. | 水分子的结构式: | B. | 氯化钠的电子式: | ||
| C. | 苯的结构简式C6H6 | D. | 硫原子的结构示意图: |
3.检验溴乙烷中含有溴元素存在的实验步骤、操作和顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
| A. | ①②④③ | B. | ②④③① | C. | ②④① | D. | ②③④① |
20.咖啡鞣酸具有抗菌作用,其结构简式如图所示.下列叙述中不正确的是( )


| A. | 咖啡鞣酸的分子式为C16H18O9 | |
| B. | 咖啡鞣酸可分别使溴水和酸性高锰酸钾溶液褪色 | |
| C. | 1mol咖啡鞣酸中含有1mol苯环 | |
| D. | 咖啡鞣酸中只含有3种官能团 |
1.下列在指定溶液中的各组离子,能够大量共存的是( )
| A. | 使无色酚酞变红的溶液中:S2-、K+、CO32-、C1- | |
| B. | 1mol•L-1的氯化铁溶液中:Na+、C1-、SCN-、Cu2+ | |
| C. | PH=0的溶液中:S2-、I-、Mg2+、Ba2+ | |
| D. | 水电离的c(H+)=10-13mol•L-1的溶液中:Fe2+、SO42-、K+、NO3- |
