题目内容
1.以下物质是按一定规律排列的,Mn、S、MnO2、SO2、K2MnO4、 ,则方框内的物质为( )
,则方框内的物质为( )| A. | H2S | B. | Na2SO3 | C. | CuSO4 | D. | Cu2S |
分析 先分析已知五种物质排布特点及含有元素化合价:Mn、MnO2、K2MnO4中Mn元素化合价分别为0、+4、+6;S、SO2中S元素的化合价分别为0、+4,则方框中S元素化合价也应该为+6价,据此对各选项进行判断.
解答 解:单质中元素的化合价是0,Mn、S中元素的化合价都是0;
氧元素为-2价,根据在化合物中正负化合价代数和为零可知MnO2中锰显+4价,SO2中硫显+4价;
钾离子为+1价,根据在化合物中正负化合价代数和为零可知,K2MnO4中锰显+6价,则锰元素的化合价应是按0、+4、+6排列的,硫元素的化合价也应是按0、+4、+6排列,
所以方框物质为含S混合物,且化合价为+6,选项中只有C符合,
故选C.
点评 本题考查了探究化学规律的方法,题目难度不大,明确已知物质含有元素及化合价变化特点为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
11.化学与日常生活、环境密切相关,下列有关说法不正确的是( )
| A. | 硅胶可作袋装食品的干燥剂 | |
| B. | 用活性炭可除去冰箱中的异味 | |
| C. | CO2、NO2、或SO2都会导致酸雨的形成 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
12.下列说法中正确的是( )
| A. | 甲烷中混有少量乙烯,可将混合气体通入盛有酸性高锰酸钾溶液的洗气瓶中除去 | |
| B. | 在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色 | |
| C. | 在苯中加入溴的四氯化碳溶液,振荡并静置后下层液体为无色 | |
| D. | 食物中含有大量的纤维素,可以在人体内直接水解成葡萄糖成为营养物质 |
9.下列离子反应不能发生的是( )
| A. | NaOH+KCl=NaCl+KOH | B. | AgNO3+NaCl=AgCl↓+NaNO3 | ||
| C. | Na2CO3+Ca(OH)2=CaCO3↓+2NaOH | D. | NaOH+NH4NO3=NaNO3+NH3•H2O |
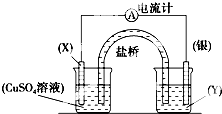 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: