题目内容
3.已知在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9kJ的热量.(1)该反应是(填“是”或“不是”)吸热反应.
(2)石墨和金刚石相比,金刚石能量高,石墨更稳定.
(3)推测石墨与金刚石各1mol在相同条件下燃烧,金刚石放出的热量多.
分析 (1)反应物的能量低于生成物能量时,反应为吸热反应;
(2)反应吸热时,反应物能量低,物质能量越低越稳定;
(3)焓变等于生成物能量与反应物能量差值.
解答 解:(1)1mol石墨转化为金刚石,吸收1.9kJ的热量,石墨转化为金刚石吸收热量,反应是吸热反应,故答案为:是;
(2)石墨生成金刚石吸热,说明石墨能量低,能量越低越稳定,石墨和金刚石相比,金刚石能量高,石墨更稳定,故答案为:金刚石;石墨;
(3)△H=生成物能量-反应物能量,因为金刚石能量高,所以相同物质的量的金刚石和石墨在相同条件下燃烧,金刚石放出的热量多,
故答案为:金刚石.
点评 本题考查了金刚石和石墨相互转化中的能量变化,理解焓变的求算、物质的能量越低越稳定等知识是解题关键,题目难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
13.如表列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是K(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素③形成的氢化物的电子式 或
或 ;
;
(3)写出上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式CCl4、PCl3.某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期第ⅥA族.
(4)写出④的最高价氧化物的水化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式3H++Al(OH)3=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
(1)以上10种元素的原子中,最容易失去电子的是K(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素③形成的氢化物的电子式
 或
或 ;
;(3)写出上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式CCl4、PCl3.某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期第ⅥA族.
(4)写出④的最高价氧化物的水化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式3H++Al(OH)3=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O.
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,18g重水(D2O)中所含的电子数为10 NA | |
| B. | 标准状况下,14g氮气含有的核外电子数为5NA | |
| C. | 标准状况下,22.4L氢气和氯气的混合气体中含有的分子总数为NA | |
| D. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移电子数为NA |
11.化学与日常生活、环境密切相关,下列有关说法不正确的是( )
| A. | 硅胶可作袋装食品的干燥剂 | |
| B. | 用活性炭可除去冰箱中的异味 | |
| C. | CO2、NO2、或SO2都会导致酸雨的形成 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
18.下列变化属于物理变化的是( )
| A. | 煤的干馏 | |
| B. | 石油裂解 | |
| C. | 煤焦油经分馏得到苯、甲苯、二甲苯等 | |
| D. | 蛋白质的变性 |
8.对氨基苯甲酸可用甲苯为原料合成,已知苯环上的硝基可被还原为氨基: ,产物苯胺还原性强,易被氧化.则由甲苯合成对氨基苯甲酸的合成路线合理的是( )
,产物苯胺还原性强,易被氧化.则由甲苯合成对氨基苯甲酸的合成路线合理的是( )
 ,产物苯胺还原性强,易被氧化.则由甲苯合成对氨基苯甲酸的合成路线合理的是( )
,产物苯胺还原性强,易被氧化.则由甲苯合成对氨基苯甲酸的合成路线合理的是( )| A. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| B. | 甲苯$\stackrel{氧化甲基}{→}$X$\stackrel{硝化}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| C. | 甲苯$\stackrel{还原}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{硝化}{→}$对氨基苯甲酸 | |
| D. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{还原硝基}{→}$Y$\stackrel{氧化甲基}{→}$对氨基苯甲酸 |
15.有相同的三块铝片,进行如下实验
实验一:取第一块铝片,直接放入硫酸铜溶液中观察现象
实验二:取第二块铝片,用砂纸擦试表面后,放入硫酸铜溶液中观察现象
实验三:将实验一中铝片从硫酸铜溶液中取出,洗净后放入氢氧化钠溶液中,片刻后取出铝片,洗净后再放入硫酸铜溶液中观察现象
实验四:取第三块铝片,用砂纸擦试表面后,置于浓硝酸中,片刻后取出,洗净,再放入硫酸铜溶液中观察现象
综合以上四个实验的主要目的是试图说明( )
实验一:取第一块铝片,直接放入硫酸铜溶液中观察现象
实验二:取第二块铝片,用砂纸擦试表面后,放入硫酸铜溶液中观察现象
实验三:将实验一中铝片从硫酸铜溶液中取出,洗净后放入氢氧化钠溶液中,片刻后取出铝片,洗净后再放入硫酸铜溶液中观察现象
实验四:取第三块铝片,用砂纸擦试表面后,置于浓硝酸中,片刻后取出,洗净,再放入硫酸铜溶液中观察现象
综合以上四个实验的主要目的是试图说明( )
| A. | 铝片能和硫酸铜溶液反应 | |
| B. | 铝片能和氢氧化钠溶液反应 | |
| C. | 铝片不能和硝酸反应 | |
| D. | 铝片表面能形成具有保护作用的氧化膜 |
12.下列说法中正确的是( )
| A. | 甲烷中混有少量乙烯,可将混合气体通入盛有酸性高锰酸钾溶液的洗气瓶中除去 | |
| B. | 在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色 | |
| C. | 在苯中加入溴的四氯化碳溶液,振荡并静置后下层液体为无色 | |
| D. | 食物中含有大量的纤维素,可以在人体内直接水解成葡萄糖成为营养物质 |
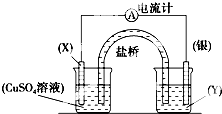 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: