题目内容
19.向FeCl2溶液中加入NaOH溶液,生成的白色沉淀迅速变成灰绿色,最后变成红褐色.分析 氯化亚铁与氢氧化钠反应生成氢氧化亚铁,为白色固体,氢氧化亚铁不稳定,易被空气中氧气氧化生成氢氧化铁,以此解答该题.
解答 解:氯化亚铁与氢氧化钠溶液反应,生成的白色絮状沉淀,发生Fe2++2OH-=Fe(OH)2↓,氢氧化亚铁不稳定,易被空气中氧气氧化生成氢氧化铁,现象是迅速变成灰绿色,最后变为红褐色,发生反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白;红褐.
点评 本题考查铁的化合物知识,为高频考点,侧重基础知识的考查,熟悉常见物质的颜色、性质、物质之间的反应即可解答,注重基础知识的考查,题目较简单.

练习册系列答案
相关题目
10.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol任何气体的体积都约是22.4 L | |
| B. | 18 g NH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量等于H3PO4的摩尔质量 | |
| D. | 标准状况下,相同体积的O2、HCl含有的分子数都为NA |
4.将浓度为0.1mol/LHF溶液加水不断稀释,下列说法正确的是( )
| A. | HF的电离平衡正向移动,c(H+)增大 | |
| B. | HF的电离程度增大,c(H+)、c(F-)增大,c(HF)减小 | |
| C. | 稀释过程中,c(OH-)增大 | |
| D. | 溶液的KW、pH均不变 |
20.核内中子数为N的R2+离子,质量数为A,则n克它的氧化物中所含质子的物质的量是( ) 摩尔.
| A. | $\frac{n(A-N+8)}{A+16}$ | B. | $\frac{n(A-N+10)}{(A+16)}$ | C. | A-N+2 | D. | $\frac{n(A-N+6)}{A}$ |
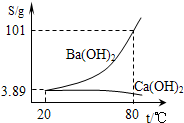 实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):