��Ŀ����
��һ����ɫ��ĩ�����п��ܺ���NaNO3��CaCl2��K2CO3����������ʵ�飺�ٽ����ַ�ĩ����ˮ�У����а�ɫ�������ɣ�����ٵ�����Һ�м������ϡ���ᣬ����ɫ������ʧ�������ݲ�������ȡ�����ڵ���Һ����AgNO3��Һ���а�ɫ�������ɣ�
��������ʵ������������и��⣺
��1��ԭ��ɫ��ĩ�п϶����е�����Ϊ �����ܺ��е�����Ϊ ��
��2��д��������з�����Ӧ�Ļ�ѧ����ʽ ��
��3��д��������з�����Ӧ�����ӷ���ʽΪ ��
��4��д��������з�����Ӧ�����ӷ���ʽ ��
��������ʵ������������и��⣺
��1��ԭ��ɫ��ĩ�п϶����е�����Ϊ
��2��д��������з�����Ӧ�Ļ�ѧ����ʽ
��3��д��������з�����Ӧ�����ӷ���ʽΪ
��4��д��������з�����Ӧ�����ӷ���ʽ
���㣺����δ֪��ļ���
ר�⣺
�������ٽ����ַ�ĩ����ˮ�У����а�ɫ�������ɣ�˵�����������ɰ�ɫ���������ʣ�
����1��������Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ�������ɫ����������̼��ƣ�
��ȡ������2������Һ����AgNO3��Һ���а�ɫ�������ɣ�֤�����������ӣ��������һ������CaCl2���Դ˽����⣮
����1��������Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ�������ɫ����������̼��ƣ�
��ȡ������2������Һ����AgNO3��Һ���а�ɫ�������ɣ�֤�����������ӣ��������һ������CaCl2���Դ˽����⣮
���
�⣺�ٽ����ַ�ĩ����ˮ�У����а�ɫ�������ɣ��ð�ɫ����Ϊ̼��ƣ�������к���CaCl2��K2CO3��
����ٵ�����Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ���������Ϊ������̼����ɫ����ΪCaCO3��
��ȡ�����ڵ���Һ����AgNO3��Һ���а�ɫ�������ɣ�֤�����������ӣ��������һ������CaCl2��
��1���������Ϸ�����֪��ԭ��ɫ��ĩ��һ�����е�����Ϊ��CaCl2��K2CO3�����ܺ���NaNO3���ʴ�Ϊ��CaCl2��K2CO3��NaNO3��
��2��������з�����Ӧ�Ļ�ѧ����ʽΪ��K2CO3+CaCl2=CaCO3��+2KCl���ʴ�Ϊ��K2CO3+CaCl2=CaCO3��+2KCl��
��3��������У���ٵ�����Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ�������Ӧ�Ļ�ѧ����ʽΪ��CaCO3+2H+=Ca2++CO2��+H2O��
�ʴ�Ϊ��CaCO3+2H+=Ca2++CO2��+H2O��
��4��������У������ڵ���Һ����AgNO3��Һ���а�ɫ�������ɣ���Ӧ�Ļ�ѧ����ʽΪ��KCl+AgNO3=AgCl��+KNO3����д�����ӷ���ʽΪ��Ag++Cl-=AgCl����
�ʴ�Ϊ��Ag++Cl-=AgCl����
����ٵ�����Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ���������Ϊ������̼����ɫ����ΪCaCO3��
��ȡ�����ڵ���Һ����AgNO3��Һ���а�ɫ�������ɣ�֤�����������ӣ��������һ������CaCl2��
��1���������Ϸ�����֪��ԭ��ɫ��ĩ��һ�����е�����Ϊ��CaCl2��K2CO3�����ܺ���NaNO3���ʴ�Ϊ��CaCl2��K2CO3��NaNO3��
��2��������з�����Ӧ�Ļ�ѧ����ʽΪ��K2CO3+CaCl2=CaCO3��+2KCl���ʴ�Ϊ��K2CO3+CaCl2=CaCO3��+2KCl��
��3��������У���ٵ�����Һ�м������ϡ���ᣬ��ɫ������ʧ���������ݲ�������Ӧ�Ļ�ѧ����ʽΪ��CaCO3+2H+=Ca2++CO2��+H2O��
�ʴ�Ϊ��CaCO3+2H+=Ca2++CO2��+H2O��
��4��������У������ڵ���Һ����AgNO3��Һ���а�ɫ�������ɣ���Ӧ�Ļ�ѧ����ʽΪ��KCl+AgNO3=AgCl��+KNO3����д�����ӷ���ʽΪ��Ag++Cl-=AgCl����
�ʴ�Ϊ��Ag++Cl-=AgCl����
���������⿼���˳������ʵ�����Ӧ�úͼ�����Ŀ�ѶȲ���Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬ע��ץס���ʵ����������ǽ����Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
235 92 |
235 92 |
A��
| ||||
B��
| ||||
C��
| ||||
D��
|
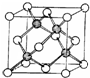 A��B��C��D��E����Ԫ�ص�ԭ������������������AΪ���ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Bԭ�ӵ��������������������������2����C�ǵؿ��к�����ߵ�Ԫ�أ�Cn-��D+������ͬ�ĵ��Ӳ�ṹ�� Eԭ�ӵ�3d�ܼ��гɶԵ�������δ�ɶԵ�����֮��Ϊ4��3���Իش��������⣺
A��B��C��D��E����Ԫ�ص�ԭ������������������AΪ���ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Bԭ�ӵ��������������������������2����C�ǵؿ��к�����ߵ�Ԫ�أ�Cn-��D+������ͬ�ĵ��Ӳ�ṹ�� Eԭ�ӵ�3d�ܼ��гɶԵ�������δ�ɶԵ�����֮��Ϊ4��3���Իش��������⣺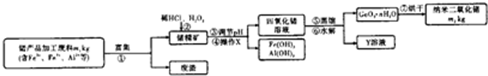
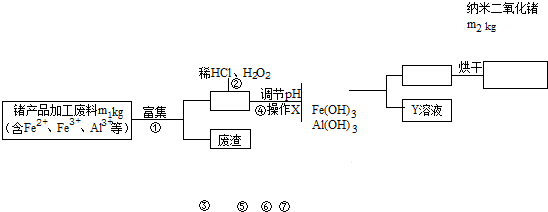
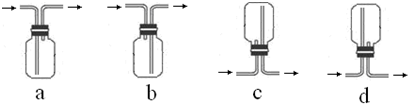
 ��ͼ��ʾ������װ�ã���ʵ���Һϳ����������Ĵֲ�Ʒ����������ƿ�ڽ��������Ҵ�������Ũ�����ϣ�Ȼ��Һ©���ߵμӴ��ᣬ�������õ������Ҵ��������ˮ�����������ֲ�Ʒ��
��ͼ��ʾ������װ�ã���ʵ���Һϳ����������Ĵֲ�Ʒ����������ƿ�ڽ��������Ҵ�������Ũ�����ϣ�Ȼ��Һ©���ߵμӴ��ᣬ�������õ������Ҵ��������ˮ�����������ֲ�Ʒ��