题目内容
工业上常以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2.
(1)已知将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,写出并配平该化学反应方程式: .
(2)在酸浸的过程中还会发生以下反应:
a.3MnO2+2FeS+6H2SO4=3MnSO4+Fe2(SO4)3+2S+6H2O
b.MnO2+CuS+4H2SO4=MnSO4+CuSO4+S+2H2O
c.Al2O3+3H2SO4=Al2(SO4)3+3H2O
将酸浸所得的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn.
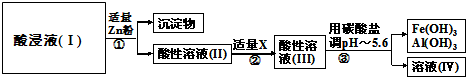
①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、
Zn+Cu2+=Zn2++Cu、 .
②操作②中加入适量X的作用是: .
③操作③中所加碳酸盐的化学式是: .
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,某化学兴趣小组设计了如下两种方案图.
方案Ⅰ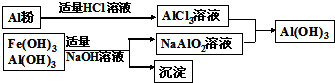
方案Ⅱ
①方案Ⅰ中,AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为: .
②从消耗酸碱的用量角度考虑,方案 (填“Ⅰ”或“Ⅱ”)所消耗的酸碱少些.
(1)已知将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,写出并配平该化学反应方程式:
(2)在酸浸的过程中还会发生以下反应:
a.3MnO2+2FeS+6H2SO4=3MnSO4+Fe2(SO4)3+2S+6H2O
b.MnO2+CuS+4H2SO4=MnSO4+CuSO4+S+2H2O
c.Al2O3+3H2SO4=Al2(SO4)3+3H2O
将酸浸所得的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn.

①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、
Zn+Cu2+=Zn2++Cu、
②操作②中加入适量X的作用是:
③操作③中所加碳酸盐的化学式是:
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,某化学兴趣小组设计了如下两种方案图.
方案Ⅰ

方案Ⅱ

①方案Ⅰ中,AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为:
②从消耗酸碱的用量角度考虑,方案
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:(1)将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,说明二氧化锰氧化硫化锌为单质硫为黄色物质,二氧化锰被还原为硫酸锰,结合原则守恒书写配平化学方程式;
(2)①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、Zn+Cu2+=Zn2++Cu、和铁离子反应生成亚铁离子;
②操作②中加入适量X的作用是沿河亚铁离子为铁离子,通过加入碳酸盐调节溶液PH使铁离子全部沉淀;
③操作③中所加碳酸盐不能引入新的杂质;
(3)①AlCl3溶液和NaAlO2溶液混合发生双水解反应生成Al(OH)3沉淀;
②分析方案Ⅰ、Ⅱ反应过程中定量关系计算分析判断需要酸碱的量的多少.
(2)①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、Zn+Cu2+=Zn2++Cu、和铁离子反应生成亚铁离子;
②操作②中加入适量X的作用是沿河亚铁离子为铁离子,通过加入碳酸盐调节溶液PH使铁离子全部沉淀;
③操作③中所加碳酸盐不能引入新的杂质;
(3)①AlCl3溶液和NaAlO2溶液混合发生双水解反应生成Al(OH)3沉淀;
②分析方案Ⅰ、Ⅱ反应过程中定量关系计算分析判断需要酸碱的量的多少.
解答:
解:(1)将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,说明二氧化锰氧化硫化锌为单质硫为黄色物质,二氧化锰被还原为硫酸锰,此反应的化学方程式为:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O;
故答案为:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O;
(2)①锌可以和H+、Cu2+、Fe3+反应,方程式为:Zn+2Fe3+=Zn2++2Fe2+,故答案为:Zn+2Fe3+=Zn2++2Fe2+;
②X是MnO2,MnO2可将Fe2+氧化成Fe3+,故答案为:将Fe2+氧化成Fe3+;
③溶液中不能引入新的杂质离子,溶液中含有锰离子和锌离子,可加入MnCO3或ZnCO3 或MnCO3和ZnCO3,可调节pH值,又不引入新的杂质,
故答案为:MnCO3或ZnCO3 或MnCO3和ZnCO3;
(3)①AlCl3溶液和NaAlO2溶液混合发生双水解反应生成AI(OH)3沉淀,反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3;
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3;
②反应流程Ⅰ:由方程式可知生成4molAI(OH)3需要1molAl3+和3molAlO2-,即由铝单质生成1molAl3+需要3mol盐酸和由氢氧化铝与氢氧化钠反应生成3molAlO2-需要3mol氢氧化钠,生成nmol氢氧化铝沉淀,即消耗的NaOH和HCl的理论量(mol)都为
,
反应流程Ⅱ,则得到同样n molAl(OH)3,根据NaAlO2+4HCl=NaCl+AlCl3+2H2O,生成nmolmolAl(OH)3消耗的HCl的理论量分别为4n mol,大于前流程的消耗量,Ⅰ流程消耗酸碱量少,故答案为:Ⅰ.
故答案为:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O;
(2)①锌可以和H+、Cu2+、Fe3+反应,方程式为:Zn+2Fe3+=Zn2++2Fe2+,故答案为:Zn+2Fe3+=Zn2++2Fe2+;
②X是MnO2,MnO2可将Fe2+氧化成Fe3+,故答案为:将Fe2+氧化成Fe3+;
③溶液中不能引入新的杂质离子,溶液中含有锰离子和锌离子,可加入MnCO3或ZnCO3 或MnCO3和ZnCO3,可调节pH值,又不引入新的杂质,
故答案为:MnCO3或ZnCO3 或MnCO3和ZnCO3;
(3)①AlCl3溶液和NaAlO2溶液混合发生双水解反应生成AI(OH)3沉淀,反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3;
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3;
②反应流程Ⅰ:由方程式可知生成4molAI(OH)3需要1molAl3+和3molAlO2-,即由铝单质生成1molAl3+需要3mol盐酸和由氢氧化铝与氢氧化钠反应生成3molAlO2-需要3mol氢氧化钠,生成nmol氢氧化铝沉淀,即消耗的NaOH和HCl的理论量(mol)都为
| 3n |
| 4 |
反应流程Ⅱ,则得到同样n molAl(OH)3,根据NaAlO2+4HCl=NaCl+AlCl3+2H2O,生成nmolmolAl(OH)3消耗的HCl的理论量分别为4n mol,大于前流程的消耗量,Ⅰ流程消耗酸碱量少,故答案为:Ⅰ.
点评:本题是一道综合题,题目难度较大,掌握铝三角相关的方程式是解题的关键.

练习册系列答案
相关题目
在制水泥、制玻璃、炼铁三种工业生产中,都需要的原料是( )
| A、纯碱 | B、石灰石 |
| C、粘土 | D、生石灰 |
下列有关实验操作说法中,正确的是( )
| A、使用干燥洁净玻璃棒将氯水滴在干燥pH试纸上,测得氯水的pH值 |
| B、葡萄糖银镜反应实验后的试管内壁附有银,可用氨水清洗 |
| C、将AlCl3溶液蒸发结晶提取无水AlCl3 |
| D、欲从碘水中分离出I2,可将适量的CCl4加入碘水中振荡静置分层后分液 |
用一种试剂区分KCl、NH4Cl、FeCl3、AlCl3,这种试剂是( )
| A、AgNO3 |
| B、HCl |
| C、NaOH |
| D、KSCN |
从海水中提取溴,主要反应为:2Br-+Cl2═Br2+2Cl-,下列说法不正确的是( )
| A、溴离子具有氧化性 |
| B、氯气是还原剂 |
| C、该反应属于复分解反应 |
| D、氯气的氧化性比溴单质强 |
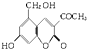 ,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题: