题目内容
2.实验室配制0.5mol/L的NaOH溶液480mL,有以下仪器:①烧杯 ②胶头滴管 ③玻璃棒 ④托盘天平(带砝码)
(1)配制时,还缺少的仪器是药匙、500mL容量瓶,实验需要称量NaOH固体10.0克
(2)实验中两次用到玻璃棒,其作用分别是:搅拌、引流.
(3)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④反复摇匀 ⑤转移
⑥洗涤 ⑦定容 ⑧冷却 ⑨初步摇匀 ⑩装入试剂瓶并贴上标签.其正确的操作顺序为:②①③⑧⑤⑥⑨⑦④⑩.
(4)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是ADF,对实验结果没有影响的是CG(填各选项的序号).
A.所用的NaOH中混有少量Na2O
B.用托盘天平称量一定质量固体NaOH时,称量时间过长.
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.定容时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面略低于刻度线,不再加蒸馏水就装入试剂瓶.
分析 (1)根据实验操作步骤确定每步操作需要仪器,然后判断还缺少仪器名称;依据m=CVM计算需要溶质的质量;
(2)根据使用玻璃棒的操作来分析其用途;
(3)据配制溶液的实验操作过程进行实验步骤排序;
(4)根据c=$\frac{n}{V}$分析操作对溶质的物质的量或对溶液的体积的影响判断.
解答 解:(1)实验室配制0.5mol/L的NaOH溶液480mL,应选择500mL容量瓶,实际配制500mL溶液,配制步骤有称量、溶解、移液、洗涤移液、定容、摇匀等操作,用天平称量NaOH(用到药匙),在烧杯中稀释,并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,
用到的仪器:烧杯、胶头滴管、玻璃棒、托盘天平(带砝码)、药匙、500mL容量瓶;
所以还缺少的仪器:药匙、500mL容量瓶;
配制500m0.5mol/L氢氧化钠溶液需要溶质的质量m=0.5mol/L×0.5 L×40g/mol=10.0g;
故答案为:药匙、500mL容量瓶 10.0;
(2)在配制过程中,溶解氢氧化钠固体时玻璃棒的用途是:搅拌,加速溶解;在移液时玻璃棒的用途是引流,
故答案为:搅拌;引流;
(3)配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀,所以正确的顺序为:②①③⑧⑤⑥⑨⑦④⑩;
故答案为:②①③⑧⑤⑥⑨⑦④⑩;
(4)A.所用的NaOH中混有少量Na2O,导致溶质氢氧化钠的物质的量偏大,溶液浓度偏高;
B.用托盘天平称量一定质量固体NaOH时,称量时间过长,导致称取的溶质质量偏小,溶质的物质的量偏小,溶液浓度偏低;
C.配制溶液所用的容量瓶洗净后没有烘干,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变;
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作,冷却后溶液体积偏小,溶液浓度偏高;
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容,导致溶质部分损耗,溶液浓度偏低;
F.定容时,俯视观察液面与容量瓶刻度线,导致溶液体积偏小,溶液浓度偏高;
G.定容摇匀后静止,发现液面略低于刻度线,不再加蒸馏水就装入试剂瓶,正确操作,溶液浓度准确;
所以将使所配制的NaOH溶液的浓度偏高的是ADF;对实验结果没有影响的是CG;
故答案为:ADF;CG.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度不大,注意掌握配制一定浓度的溶液操作步骤,注意容量瓶规格选择及使用方法.

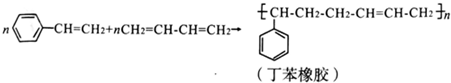
下列有关说法错误的是( )
| A. | 丁苯橡胶的两种单体都属于烃 | B. | 丁苯橡胶不能使溴水褪色 | ||
| C. | 上述反应的原子利用率为100% | D. | 丁苯橡胶属于高分子化合物 |
| A. | 苯不与溴水发生加成反应 | |
| B. | 苯不与酸性KMnO4溶液反应 | |
| C. | 1 mol 苯可与3 mol H2发生加成反应 | |
| D. | 苯燃烧时冒黑烟 |
| A. | 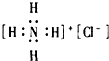 | B. | 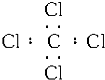 | C. | 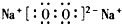 | D. | 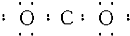 |
| A. | 消耗2molM 的同时生成2mol Q | |
| B. | 反应混合物中Q的物质的量不再改变 | |
| C. | M与Q体积相等 | |
| D. | M、N、Q的物质的量之比为2:1:2 |
 、醛基-CHO、羧基-COOH.
、醛基-CHO、羧基-COOH.