题目内容
16.“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式的划时代的意义.请回答下列问题:
(1)无机非金属材料
高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:
SiO2$→_{高温}^{Ⅰ.C}$Si(粗)$→_{300℃}^{Ⅱ.HCl}$SiHCl3$→_{1000℃-1100℃}^{Ⅲ.过量H_{2}}$Si(纯)
①写出步骤Ⅰ的化学方程式:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
②步骤Ⅱ经过冷凝得到的SiHCl3(沸点为33.0℃)中含有少量的SiCl4(沸点为57.6℃)和HCl(沸点为-84.7℃),提纯SiHCl3的实验方法是蒸馏或分馏.
(2)磁性材料
这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施对它的防护.最常见的铁制品腐蚀是电化学腐蚀,请写出最为普遍的电化学腐蚀的负极反应式:Fe-2e-=Fe2+.
(3)激光材料
我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:Al2O3+6H+═2Al3++3H2O、Al2O3+2OH-+3H2O=2[Al(OH)4]-.
(4)高分子材料
它可以分成无机高分子材料和有机高分子材料.一种新型高效净水剂[AlFe(OH)nCl6-n]m就属于无机高分子材料,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3;一种合成纤维腈纶,又称“人造羊毛”,以丙烯腈(CH2═CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式:
 .
.(5)合金材料
14g铜银合金与一定量某浓度的硝酸完全反应后,将放出的气体与1.12L(标准状况下)O2混合通入水中,恰好全部被水吸收,则合金中铜的质量为3.2 g.
分析 (1)①焦炭在高温下可以置换二氧化硅中的硅;
②根据熔沸点的不同实现物质分离的方法为蒸馏或分馏;
(2)在铁制品腐蚀的电化学腐蚀中,金属铁作负极发生氧化反应;
(3)氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,均放出氢气;
(4)AlFe(OH)nCl6-n中各元素的化合价代数和为0,丙烯腈(CH2=CH-CN)中的双键能发生加聚反应;
(5)铜、银合金与足量的某浓度的硝酸反应,硝酸所起作用为酸性和氧化性,起酸性作用的硝酸生成硝酸铜、硝酸银,起氧化性作用的硝酸被还原为氮的氧化物(无法确定具体物质),氮的氧化物与氧气混合通入水中,反应又生成硝酸,根据氮元素守衡,该硝酸的量恰好等于起氧化性作用的硝酸的量.所以有铜、银合金失去的电子总数等于氧气获得的电子总数.利用铜、银合金失去的电子总数等于氧气获得的电子总数以及铜、银合金总质量为14g,列方程求解.
解答 解:(1)①工业上用焦炭在高温下置换二氧化硅中的硅来制备粗硅,方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
②SiHCl3(沸点33.0℃)、SiCl4(沸点57.6℃)、HCl(沸点-84.7℃),他们的沸点不同,根据沸点的不同实现物质分离的方法为蒸馏或分馏,故答案为:蒸馏或分馏;
(2)在铁制品的电化学腐蚀中,金属铁作负极发生氧化反应,电极反应为:Fe-2e-→Fe2+,
故答案为:Fe-2e-→Fe2+;
(3)氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,
故答案为:Al2O3+6H+═2Al3++3H2O、Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(4)化合物中铝元素显+3价,氢氧根为-1价,各元素的化合价代数和为0,故铁元素的化合价为+3价,丙烯腈(CH2=CH-CN)中的双键能发生加聚反应,方程式为: ,故答案为:+3;
,故答案为:+3; ;
;
(5)n(O2)=$\frac{1.12g}{22.4g/mol}$=0.05mol
设Cu、Ag的物质的量分别为x、y,则:
根据质量列方程:x×64g/mol+y×108g/mol=14g
根据电子守恒列方程:2x+1×y=0.05mol×4
解得:x=0.05mol;y=0.1mol
m(Cu)=0.05mol×64g/mol=3.2g,
故答案为:3.2g.
点评 本题是一道有关硅的无机推断题,考查的知识点范围较广,涉及原电池、两性氧化物、高分子材料、氧化还原反应的计算等,题目难度中等.

| A. | 活化分子间的碰撞一定能发生化学反应 | |
| B. | 升高温度时,化学反应速率加快,主要原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 | |
| C. | 自发进行的反应一定迅速 | |
| D. | 凡是熵增加的过程都是自发过程 |
发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}/△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
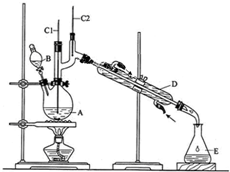
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,易迸溅.
(2)加入沸石的作用是防止暴沸.
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是冷凝管.
(4)分液漏斗使用前必须进行的操作是c(填正确答案标号).
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在下层(填“上”或“下”).
(6)本实验中,纯净的正丁醛的检验方法:利用质谱仪测定相对分子质量.
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是蒸馏烧瓶.
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加B.冷却后补加C.不需补加D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是吸收水.
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有BE(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是61%.(保留两位有效数字)
(注:产率=实际产量/理论产量×100%)
| A. | 25℃、101KPa时,16g O2和O3混合气体中含有的原子数为NA | |
| B. | 1 mol NH3中含有的质子数为17NA | |
| C. | 11.2 L O2和N2的混合气体含有的分子数为0.5NA | |
| D. | 金属铁与稀盐酸反应当产生0.1 mol H2时转移电子数为0.3NA |
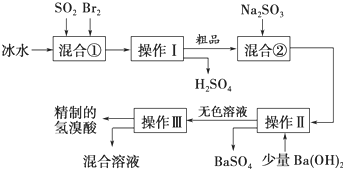
 某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验:
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验: