题目内容
在同温同压下,A容器中盛有H2,B容器中盛有NH3,若使它们所含的原子数相等,则两个容器的体积之比是( )
| A、2:1 | B、1:5 |
| C、2:3 | D、5:1 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:在同温同压下,气体的体积之比等于物质的量之比,设A、B的体积分别为x、y,结合物质的构成及它们所含的原子数相等解答.
解答:
解:在同温同压下,气体的体积之比等于物质的量之比,设A、B的体积分别为x、y,
由原子数相等可知,
x×2=y×4,
则x:y=2:1,
故选A.
由原子数相等可知,
x×2=y×4,
则x:y=2:1,
故选A.
点评:本题考查阿伏伽德罗定律及其推论,明确相同条件下体积与物质的量的关系是解答关键,把握原子数目的关系,题目难度不大.

练习册系列答案
相关题目
在水溶液中能大量共存的一组离子是( )
| A、Fe2+、Al3+、ClO-、Cl- |
| B、K+、Ba2+、OH-、NO3- |
| C、NH4+、Na+、OH-、SO42- |
| D、Mg2+、H+、SiO32-、SO42- |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、16 g CH4中含有4 nA个C-H键 |
| B、1 mol/L NaCl溶液含有nA个Na+ |
| C、1 mol Cu和足量稀硝酸反应产生nA个NO分子 |
| D、标准状况下,22.4 L 己烯中含有nA个己烯分子 |
a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列物质属于钠盐的是( )
| A、Na2O |
| B、Na2O2 |
| C、NaOH |
| D、CH3COONa |
在加入铝粉能产生H2的溶液中下列各组离子可能大量共存的是( )
| A、NH4+ NO3- CO32- Na+ |
| B、Na+ Ba2+ Mg2+ HCO3- |
| C、NO3- Mg2+ K+ Cl- |
| D、NO3- K+ AlO2- OH- |
下列物质类别、名称(或俗名)、化学式相符的是( )
| A、碱性氧化物,氧化亚铁,Fe2O3 |
| B、酸,硫酸,H2SO3 |
| C、碱,熟石灰,CaO |
| D、酸性氧化物,干冰,CO2 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、0.5 L 1 mol/L的Na2SO4溶液中,含有Na+的个数为NA |
| B、22.4 L N2含有氮原子的个数为2NA |
| C、1 mol钠与水反应生成氢气的分子数为0.5NA |
| D、NA个Cl2分子与水反应,转移的电子数为2NA |
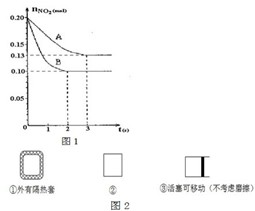 在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.
在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.