题目内容
18.苹果酸结构简式为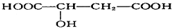 ,苹果酸可能发生的反应是( )
,苹果酸可能发生的反应是( )①与NaOH溶液反应
②与石蕊试液作用变红
③与金属钠反应放出气体
④一定条件下能发生消去反应
⑤一定条件下能发生氧化反应.
| A. | ①②③ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
分析 由结构可知,分子中含-OH、-COOH,结合醇、羧酸的性质来解答.
解答 解:含-COOH,与NaOH发生中和反应,与石蕊试液作用变红,与Na反应生成氢气;
含-OH,与金属钠反应放出气体,一定条件下能发生消去反应,一定条件下能发生氧化反应,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意醇、羧酸的性质,题目难度不大.

练习册系列答案
相关题目
8.下列有关化学用语的说法不正确的是( )
| A. | -OH与 都表示羟基 都表示羟基 | B. | 如图是食盐晶体的晶胞 | ||
| C. | CH4分子的球棍模型: | D. | 次氯酸分子的电子式: |
9.下列图示与对应的叙述相符的是( )
| A. |  表示某吸热反应分别在有、无催化剂的情况况下反应过程中的能量变化 | |
| B. |  表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的物质的量与NaOH溶液体积的关系,则三种离子的物质的量之比比为(Mg2+):(Al3+):n(NH4+)=2:3:2 | |
| C. | 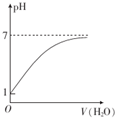 表示常温下0.10 mol•L-1的CH3COOH溶液加水稀释时溶液的pH变化 | |
| D. |  表示向10.00 mL 0.050 mol•L-1盐酸中逐滴加人0.025 mol•L-1的氨水时溶液的pH变化,其中 V1>20.00 |
13.下列化学键中,键的极性最强的是( )
| A. | H-F | B. | H-O | C. | H-N | D. | H-C |
3.常温下,下列叙述正确的是( )
| A. | K2CO3溶液中,$\frac{1}{2}$c(K+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 某浓度的NaAc溶液的pH=8,则该溶液中的c(Na+)-c(Ac-)=9.9×10-7mol/L | |
| C. | 物质的量浓度相等的①NH4Cl、②(NH4)2SO4两种溶液,c(NH4+)大小顺序为:①>② | |
| D. | 10mLpH=12的烧碱溶液中加入pH=2的酸HA至中性,所需酸溶液的体积V≥10mL |
10.某的化合物化学式为:K3[Fe(C2O4)3],下列有关说法正确的是( )
| A. | 铁元素的化合价是+3 | |
| B. | 铁离子的配位数是3 | |
| C. | C2O42-中碳原子的杂化方式为sp3 | |
| D. | 该物质中含有离子键,配位键和极性共价键 |
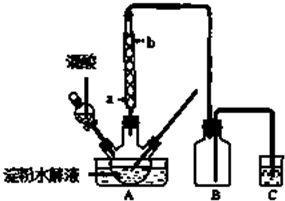
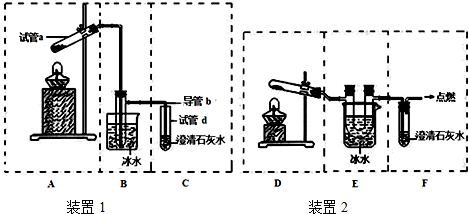
 .
.