题目内容
实验室:可用下列药品:浓硫酸、KClO3、MnO2和浓盐酸制备A、B和C三种常见气体.
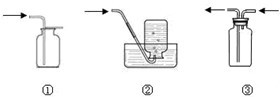
(1)若要制备一种无色无味的气体A.可选择下图装置中的 ( 填序号)收集干燥气体A.
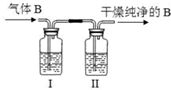
(2)在实验中要获得干燥纯净的黄绿色气体B,可以将制得不纯净的B气体通过下图中的装置,其中瓶I中盛放的是 ,瓶Ⅱ中盛放的是 .
(3)写出实验室常用于制备B气体的离子方程式 .
(4)实验中必须吸收多余的气体,以免污染空气,下图是实验室用水吸收无色有刺激性气味的气体C的装置,为防止发生倒吸现象,合理的装置是 (填序号).

(5)将气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,请对B的水溶液中哪一种粒子能使石蕊试液褪色提出合理假设;
假设一:只有Cl2能使石蕊试液褪色
假设二: ;
假设三: ;
选择合适的仪器和药品(试剂或试纸)来验证假设一是否成立.
(1)若要制备一种无色无味的气体A.可选择下图装置中的

(2)在实验中要获得干燥纯净的黄绿色气体B,可以将制得不纯净的B气体通过下图中的装置,其中瓶I中盛放的是

(3)写出实验室常用于制备B气体的离子方程式
(4)实验中必须吸收多余的气体,以免污染空气,下图是实验室用水吸收无色有刺激性气味的气体C的装置,为防止发生倒吸现象,合理的装置是

(5)将气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,请对B的水溶液中哪一种粒子能使石蕊试液褪色提出合理假设;
假设一:只有Cl2能使石蕊试液褪色
假设二:
假设三:
选择合适的仪器和药品(试剂或试纸)来验证假设一是否成立.
| 仪器和药品 | 步骤 | 现象 | 结论 |
考点:常见气体制备原理及装置选择
专题:实验题,实验设计题
分析:KClO3和MnO2加热可以制取氧气,二氧化锰和浓盐酸可以制取氯气,浓硫酸和氯酸钾分解的氯化钾制取氯化氢气体.由于A为无色无味气体,故A为氧气;B为黄绿色气体,故B为氯气;C为无色有刺激气味气体,故C为HCl气体.
(1)氧气的密度比空气密度大,又要收集干燥气体,故用向上排空气法收集氧气;
(2)收集干燥纯净的氯气可以先通过饱和食盐水除去混有的氯化氢气体,再通过浓硫酸除去水分;
(3)制取氯气使用二氧化锰和浓盐酸反应制取;
(4)①导管离液面太远不利于吸收,②导管深入到液面一下,不能防倒吸,③干燥管可以使液体在重力作用下落回水槽,防止倒吸,④使气体不和水接触,起到防倒吸的作用;
(5)气体C在水溶液中存在Cl-、H+,气体B在水溶液中存在Cl-、H+、气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,可推知使石蕊试液褪色的可能是ClO-、HClO、Cl2.
(1)氧气的密度比空气密度大,又要收集干燥气体,故用向上排空气法收集氧气;
(2)收集干燥纯净的氯气可以先通过饱和食盐水除去混有的氯化氢气体,再通过浓硫酸除去水分;
(3)制取氯气使用二氧化锰和浓盐酸反应制取;
(4)①导管离液面太远不利于吸收,②导管深入到液面一下,不能防倒吸,③干燥管可以使液体在重力作用下落回水槽,防止倒吸,④使气体不和水接触,起到防倒吸的作用;
(5)气体C在水溶液中存在Cl-、H+,气体B在水溶液中存在Cl-、H+、气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,可推知使石蕊试液褪色的可能是ClO-、HClO、Cl2.
解答:
解:KClO3和MnO2加热可以制取氧气,二氧化锰和浓盐酸可以制取氯气,浓硫酸和氯酸钾分解的氯化钾制取氯化氢气体.由于A为无色无味气体,故A为氧气;B为黄绿色气体,故B为氯气;C为无色有刺激气味气体,故C为HCl.
(1)氧气的密度比空气密度大,又要收集干燥气体,故用向上排空气法收集氧气,故答案为:①;
(2)收集干燥纯净的氯气可以先通过饱和食盐水除去气体中混有的氯化氢气体,再通过浓硫酸除去气体中混有的水分,故答案为:饱和食盐水;硫酸;
(3)制取氯气使用二氧化锰和浓盐酸反应制取,反应的离子方程式为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
(4))①导管离液面太远不利于吸收,②导管深入到液面一下,不能防倒吸,③干燥管可以使液体在重力作用下落回水槽,防止倒吸,④使气体不和水接触,起到防倒吸的作用,故答案为:③④;
(5)气体C在水溶液中存在Cl-、H+,气体B在水溶液中存在Cl-、H+、气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,可推知使石蕊试液褪色的可能是ClO-、HClO、Cl2.验证假设一时不能用湿润的氯气实验,因为氯气和水反应有ClO-、HClO生成,必须使用干燥洁净的氯气和干燥的石蕊试纸进行实验,若干燥额蓝色石蕊试纸不变色证明氯气不能使蓝色石蕊试液褪色.
故答案为:假设二:只有ClO-能使石蕊试液褪色 假设三:只有HClO能使石蕊试液褪色
(1)氧气的密度比空气密度大,又要收集干燥气体,故用向上排空气法收集氧气,故答案为:①;
(2)收集干燥纯净的氯气可以先通过饱和食盐水除去气体中混有的氯化氢气体,再通过浓硫酸除去气体中混有的水分,故答案为:饱和食盐水;硫酸;
(3)制取氯气使用二氧化锰和浓盐酸反应制取,反应的离子方程式为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
(4))①导管离液面太远不利于吸收,②导管深入到液面一下,不能防倒吸,③干燥管可以使液体在重力作用下落回水槽,防止倒吸,④使气体不和水接触,起到防倒吸的作用,故答案为:③④;
(5)气体C在水溶液中存在Cl-、H+,气体B在水溶液中存在Cl-、H+、气体C通入紫色石蕊试液时只变红,而通入B气体则先变红再褪色,可推知使石蕊试液褪色的可能是ClO-、HClO、Cl2.验证假设一时不能用湿润的氯气实验,因为氯气和水反应有ClO-、HClO生成,必须使用干燥洁净的氯气和干燥的石蕊试纸进行实验,若干燥额蓝色石蕊试纸不变色证明氯气不能使蓝色石蕊试液褪色.
故答案为:假设二:只有ClO-能使石蕊试液褪色 假设三:只有HClO能使石蕊试液褪色
| 仪器和药品 | 步骤 | 现象 | 结论 |
| 干燥纯净的氯气和干燥的蓝色石蕊试纸 | 将干燥的蓝色石蕊试纸放入一个充满干燥纯净的氯气的集气瓶中 | 干燥的蓝色石蕊试纸不变色 | 氯气不能使蓝色石蕊试液褪色 |
点评:本题考查了中学常见气体的收集方法、制取原理及其性质,难度不大,注意使石蕊试液褪色的是次氯酸而不是氯气.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
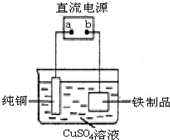 铁在地壳中的含量约占 5%左右.铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是 Fe2O3)等.
铁在地壳中的含量约占 5%左右.铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是 Fe2O3)等.
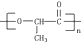 由一种单体缩聚而成的,该单体的结构简式为
由一种单体缩聚而成的,该单体的结构简式为 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.