题目内容
废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(S)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ?mol-1
2H2O2(I)═2H2O(I)+O2(g)△H=-196kJ?mol-1
2H2(g)+O2(g)═2H2O(I)△H=-570kJ?mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 .
(2)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol?L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
当温度高于 40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 .
(3)在提纯后CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是 .
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(S)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ?mol-1
2H2O2(I)═2H2O(I)+O2(g)△H=-196kJ?mol-1
2H2(g)+O2(g)═2H2O(I)△H=-570kJ?mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
(2)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol?L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率 (×10-3mol?L-1?min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
(3)在提纯后CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是
考点:热化学方程式,化学反应速率的影响因素
专题:化学反应中的能量变化,化学反应速率专题
分析:(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)根据图示信息,当温度升高时反应速率加快来回答;
(3)根据反应物和生成物来书写离子反应.
(2)根据图示信息,当温度升高时反应速率加快来回答;
(3)根据反应物和生成物来书写离子反应.
解答:
解:(1):①Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ/mol,
②2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ/mol,
③2H2(g)+O2(g)═2H2O(I)△H=-570kJ?mol-1,
由盖斯定律①+
×②+③×
得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol;
故答案为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol;
(2)根据测得不同温度下铜的平均溶解速率的数据,会发现随着温度的升高,铜的平均溶解速率,当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,因为双氧水受热易分解,导致金属铜的反应速率减慢,
故答案为:H2O2分解速率加快;
(3)根据题干信息,可知发生的反应为2Cu2++SO32-+2Cl-+H2O
2CuCl↓+SO42-+2H+,
故答案为:2Cu2++SO32-+2Cl-+H2O
2CuCl↓+SO42-+2H+.
②2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ/mol,
③2H2(g)+O2(g)═2H2O(I)△H=-570kJ?mol-1,
由盖斯定律①+
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol;
(2)根据测得不同温度下铜的平均溶解速率的数据,会发现随着温度的升高,铜的平均溶解速率,当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,因为双氧水受热易分解,导致金属铜的反应速率减慢,
故答案为:H2O2分解速率加快;
(3)根据题干信息,可知发生的反应为2Cu2++SO32-+2Cl-+H2O
| ||
故答案为:2Cu2++SO32-+2Cl-+H2O
| ||
点评:本题考查热化学方程式和盖斯定律计算应用,铜的化合物的性质,是一道综合题目,难度中等,要求学生具有分析和解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、HCO3-、C1-、K+ |
| C、Fe3+、K+、I-、H+ |
| D、H+、Cl-、Na+、CO32- |
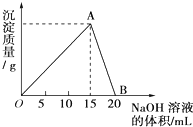 向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示: