题目内容
20.在标准状况下,将0.1mol Al投入到1L0.1mol/的稀硫酸中充分反应,下列说法不正确的是( )| A. | 该反应中Al是还原剂,稀硫酸是氧化剂 | |
| B. | 该反应中消耗Al的质量为1.8g | |
| C. | 生成2.24L H2 | |
| D. | 该反应中有0.3NA个电子发生转移 |
分析 A、铝与稀硫酸反应生成硫酸铝和氢气,铝是还原剂,硫酸是氧化剂;
B、0.1mol Al转移0.3mol的电子,而1L0.1mol/L的硫酸的物质的量为:0.1mol,转移0.2mol的电子,所以铝过量,而参加反应的铝为0.1mol×$\frac{2}{3}$;
C、在标准状况下,生成0.1mol的氢气;
D、由B可知铝过量,硫酸不足完全反应.
解答 解:A、铝与稀硫酸反应生成硫酸铝和氢气,铝是还原剂,硫酸是氧化剂,故A正确;
B、0.1mol Al转移0.3mol的电子,而1L0.1mol/L的硫酸的物质的量为:0.1mol,转移0.2mol的电子,所以铝过量,而参加反应的铝为0.1mol×$\frac{2}{3}$,所以质量为:0.1mol×$\frac{2}{3}$×27g/mol=1.8g,故B正确;
C、在标准状况下,生成0.1mol的氢气,氢气的体积为:2.24L,故C正确;
D、由B可知铝过量,硫酸不足完全反应,所以转移电子数为:0.2NA个,故D错误;
故选D.
点评 本题考查氧化还原反应的相关知识,涉及过量问题的判断,和氧化还原反应中基本概念的考查,比较容易.

练习册系列答案
相关题目
11.乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
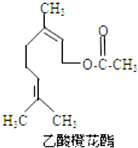

| A. | 分子式为C12H22O2 | |
| B. | 能使酸性KMnO4溶液褪色,能发生加成反应,但不能发生取代反应 | |
| C. | 1mol该有机物水解时只能消耗 1 mol NaOH | |
| D. | 1mol该有机物在一定条件下和H2反应,共消耗 H2为3mol |
8.向1L、0.4mol/LH2SO4溶液中加入10.1gKNO3和9.6g铜粉,充分反应后产生的气体在标准状况下的体积为( )
| A. | 2.24L | B. | 3.36L | C. | 4.48L | D. | 5.60L |
15.下列反应中,S元素的化合价升高的是( )
| A. | Zn+H2SO4═ZnSO4+H2↑ | |
| B. | C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O | |
| C. | H2S+CuSO4═CuS↓+H2SO4 | |
| D. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
5.关于氧气(O2)和臭氧(O3)说法正确的是( )
| A. | 互为同素异形体 | |
| B. | 二者相互转化是物理变化 | |
| C. | 同温同压下,等体积的氧气和臭氧含有相同的分子数 | |
| D. | 等物质的量的氧气和臭氧含有相同的质子数 |
12.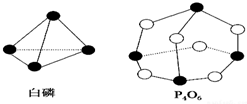 化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
 化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )| A. | 吸收1638kJ能量 | B. | 放出1638kJ能量 | C. | 吸收126kJ能量 | D. | 放出126kJ能量 |
9.下列叙述正确的是( )
(1)c(H+)═c(OH-)=10-6mol/L的溶液一定呈中性
(2)已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
(3)向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
(4)同一主族的元素,原子半径越大,其单质的熔点不一定越高
(5)乙酸乙酯在NaOH溶液(H218O)中水解产物为CH3CO18ONa和CH3CH2OH
(6)水的电子式 H+[:O:]2-H+.
(1)c(H+)═c(OH-)=10-6mol/L的溶液一定呈中性
(2)已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
(3)向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
(4)同一主族的元素,原子半径越大,其单质的熔点不一定越高
(5)乙酸乙酯在NaOH溶液(H218O)中水解产物为CH3CO18ONa和CH3CH2OH
(6)水的电子式 H+[:O:]2-H+.
| A. | (1)(2)(5)(6) | B. | (1)(4)(5) | C. | (2)(4)(6) | D. | 全部 |
10.下列物质由CH2═CH-CH2-CH3与Br2加成得到的是( )
| A. | CH3CH2CHBrCH2Br | B. | CH3CHBrCHBrCH3 | C. | 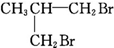 | D. | 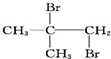 |