题目内容
12.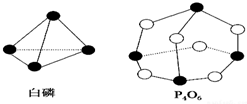 化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,若生成1mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )| A. | 吸收1638kJ能量 | B. | 放出1638kJ能量 | C. | 吸收126kJ能量 | D. | 放出126kJ能量 |
分析 反应热△H=反应物总键能-生成物总键能,据此计算判断.注意每摩尔P4中含有6molP-P键.
解答 解:各化学键键能为P-P 198kJ•mol-1、P-O 360kJ•mol-1、O=O 498 kJ•mol-1.
反应热△H=反应物总键能-生成物总键能,由图可知:1个P分子中含有6个P-P,1个P4O6分子中含有12个P-O.1mol P4和3mol O2完全反应(P4+3O2=P4O6)生成1mol P4O6,所以反应P4+3O2=P4O6的反应热△H=6×198kJ•mol-1+3×498kJ•mol-1-12×360kJ•mol-1=-1638kJ•mol-1,反应放热1638kJ,
故选:B.
点评 本题考查反应热与化学键键能的关系,难度中等,注意从物质能量、键能理解反应热.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
2.下列反应中,属于加成反应的是( )
| A. | 甲烷与氯气混合,光照一段时间后黄绿色消失 | |
| B. | 乙烯使溴水褪色 | |
| C. | 将苯滴入少量到溴水中,振荡后水层接近无色 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色 |
3.关于有机物的说法正确的是( )
| A. | 甲烷是一种很清洁的能源,它是液化石油气和天然气的主要成分 | |
| B. | 用高锰酸钾浸泡过的砖块可使水果保鲜,是利用了乙烯的还原性 | |
| C. | 苯不能使酸性高锰酸钾溶液褪色,说明它是一种饱和烃,很稳定 | |
| D. | 交警用重铬酸钾检查司机是否酒后驾车,是利用了乙醇的氧化性 |
20.在标准状况下,将0.1mol Al投入到1L0.1mol/的稀硫酸中充分反应,下列说法不正确的是( )
| A. | 该反应中Al是还原剂,稀硫酸是氧化剂 | |
| B. | 该反应中消耗Al的质量为1.8g | |
| C. | 生成2.24L H2 | |
| D. | 该反应中有0.3NA个电子发生转移 |
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 加热条件下,1 mol Cl2与足量铁粉充分反应,转移的电子数为3NA | |
| B. | 1 L 1 mol/L的Na2CO3溶液中所含Na+ 离子数为NA | |
| C. | 标准状况下,11.2 L H2O中含有的电子数为5NA | |
| D. | 1 mol CO2和O2的混合气体中所含氧原子数为2NA |
17.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是( )
| A. | HCl | B. | NO | C. | NH3 | D. | Cl2 |
1.下列对于“摩尔”的理解正确的是( )
| A. | 摩尔是国际单位制的七个物理量之一 | |
| B. | 摩尔是表示物质质量的单位 | |
| C. | 科学上规定含有阿伏加德罗常数个粒子的任何粒子集合体为1mol | |
| D. | 1mol氧含6.02×1023个O2 |
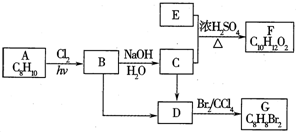 A~G都是有机化合物,它们的转化关系如下:
A~G都是有机化合物,它们的转化关系如下:
 .
. (结构简式)
(结构简式)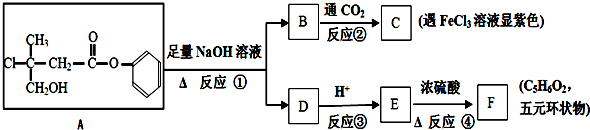
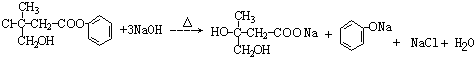 .
.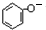 +CO2+H2O→
+CO2+H2O→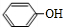 +HCO3-.
+HCO3-. .
.