题目内容
11.某同学为配置含有X,SO42-,Mg2+,NO3-四种离子的无色溶液,要使四种离子的物质的量浓度之比为1:2:1:1,则X应该是:( )| A. | Fe3+ | B. | Al3+ | C. | NH4+ | D. | Cl- |
分析 根据溶液不显电性,则所有阳离子带的正电荷总数等于阴离子带的负电荷总数,从而计算出离子的电荷数,再利用离子共存来分析解答.
解答 解:因溶液不显电性,阳离子带的正电荷总数等于阴离子带的负电荷总数,
NO3-与SO42-的电荷总数为1×1+2×2=5,
Mg2+的电荷总数为2×1=2,
显然阴离子总数大于Mg2+的电荷总数,
则X为阳离子,
设X带的电荷数位x,
由物质的量之比为n(NO3-):n(SO42-):n(Mg2+):n(X)=1:2:1:1,
则1×1+2×2=2×1+1×x,
解的x=+3,
无色溶液所以不可能是铁离子,只有铝离子符合,
故选B.
点评 本题考查溶液中离子的成分,明确溶液的电中性及离子之间的反应即可解答,难度不大,但学生容易忽略离子共存而错选.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
1.乙苯是一种用途广泛的有机原料,可制备多种化工产品.
(一)制备苯乙烯(原理如反应I所示):
Ⅰ、 ?
? (g)+H2(g)△H=+124kJ•mol-1
(g)+H2(g)△H=+124kJ•mol-1
(1)部分化学键的键能如下表所示:
根据反应I的能量变化,计算x=612.
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气.用化学一平衡理论解释通入水蒸气的原因为正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率.
(3)从体系自由能变化的角度分析,反应I在高温(填“高温”或“低温”)下有利于其自发进行.
(二)制备α-氯乙基苯(原理如反应Ⅱ所示):
Ⅱ、 +Cl2(g)?
+Cl2(g)? +HCl(g)△H2>0
+HCl(g)△H2>0
(4)T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,乙苯或Cl2、α-氯乙基苯或HCl的物质的量浓度(c)随时间(t)变化的曲线如图l所示:

①0-5min内,以HCl表示的该反应速率v(HCl)=0.032mol•L-1•min-1.
②T℃时,该反应的平衡常数K=16.
③6min时,改变的外界条件为升高温度.
④10min时,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,12min时达到新平衡.在图2中画出10-12min,Cl2和HC1的浓度变化曲线(曲线上标明Cl2和HC1);0-5min和0-12min时间段,Cl2的转化率分别用α1、α2表示,则αl<α2(填“>”、“<”或“=”).
(一)制备苯乙烯(原理如反应I所示):
Ⅰ、
 ?
? (g)+H2(g)△H=+124kJ•mol-1
(g)+H2(g)△H=+124kJ•mol-1(1)部分化学键的键能如下表所示:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | x | 436 |
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气.用化学一平衡理论解释通入水蒸气的原因为正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率.
(3)从体系自由能变化的角度分析,反应I在高温(填“高温”或“低温”)下有利于其自发进行.
(二)制备α-氯乙基苯(原理如反应Ⅱ所示):
Ⅱ、
 +Cl2(g)?
+Cl2(g)? +HCl(g)△H2>0
+HCl(g)△H2>0(4)T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,乙苯或Cl2、α-氯乙基苯或HCl的物质的量浓度(c)随时间(t)变化的曲线如图l所示:

①0-5min内,以HCl表示的该反应速率v(HCl)=0.032mol•L-1•min-1.
②T℃时,该反应的平衡常数K=16.
③6min时,改变的外界条件为升高温度.
④10min时,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,12min时达到新平衡.在图2中画出10-12min,Cl2和HC1的浓度变化曲线(曲线上标明Cl2和HC1);0-5min和0-12min时间段,Cl2的转化率分别用α1、α2表示,则αl<α2(填“>”、“<”或“=”).
19.完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
| A. |  从KI和I2的固体混合物中回收I2 | |
| B. |  除去乙醇中的苯酚 | |
| C. |  实验用CCl4提取溴水中的Br2 | |
| D. |  配制100mL 0.1000mol•L-1 K2Cr2O7溶液 |
6.实验室从含氯化钠、硝酸钾混合液中提取KNO3的过程如图所示.下列分析正确的是( )


| 选项 | 操作1 | 操作2 | 操作3 | 操作4 |
| A | 溶解 | 结晶 | 蒸发 | 过滤 |
| B | 蒸发 | 过滤 | 冷却 | 过滤 |
| C | 蒸发 | 结晶 | 结晶 | 蒸发 |
| D | 过滤 | 结晶 | 冷却 | 结晶 |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关实验及其分析叙述正确的是( )
| A. | 向2.0mL浓度均为0.lmol•L-l的KC1、KI混合溶液中滴加1~2滴0.0lmol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比Agl的Ksp大 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入适量的H2O2,铜粉仍不溶解 | |
| C. | 向AIC13溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀不消失 | |
| D. | 将CO2通入Ba(NO3)2溶液中至饱和,无沉淀产生;再通入SO2,也无沉淀产生 |
3.制备硅单质时,主要化学反应如下:
(1)SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si(粗硅)+2CO
(2)Si(粗)+2Cl2$\frac{\underline{\;加热\;}}{\;}$SiCl4
(3)SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$ Si (纯)+4HCl
对上述三个反应叙述中,不正确的是( )
(1)SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si(粗硅)+2CO
(2)Si(粗)+2Cl2$\frac{\underline{\;加热\;}}{\;}$SiCl4
(3)SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$ Si (纯)+4HCl
对上述三个反应叙述中,不正确的是( )
| A. | (1)(3)为置换反应 | B. | (1)(2)(3)均为氧化还原反应 | ||
| C. | (2)为化合反应 | D. | 反应物中硅元素均被还原 |
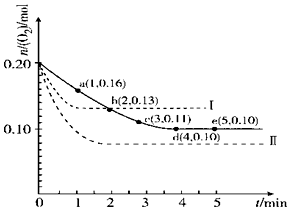 一定温度下,在2L的密闭容器中充入0.4mol SO2和0.2mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(O2)随时间的变化关系如图实线所示:
一定温度下,在2L的密闭容器中充入0.4mol SO2和0.2mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(O2)随时间的变化关系如图实线所示:
 如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.
如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.