题目内容
6.实验室从含氯化钠、硝酸钾混合液中提取KNO3的过程如图所示.下列分析正确的是( )
| 选项 | 操作1 | 操作2 | 操作3 | 操作4 |
| A | 溶解 | 结晶 | 蒸发 | 过滤 |
| B | 蒸发 | 过滤 | 冷却 | 过滤 |
| C | 蒸发 | 结晶 | 结晶 | 蒸发 |
| D | 过滤 | 结晶 | 冷却 | 结晶 |
| A. | A | B. | B | C. | C | D. | D |
分析 从含氯化钠、硝酸钾混合液中提取KNO3,二者溶解度受温度影响不同,结合流程可知,操作1为蒸发,操作2为过滤分离出NaCl,操作3为冷却结晶,操作4为过滤,以此来解答.
解答 解:因二者溶解度受温度影响不同,NaCl的溶解度受温度影响不大,而硝酸钾的溶解度受温度影响较大,结合流程可知,操作1为蒸发,操作2为过滤分离出NaCl,操作3为冷却结晶,操作4为过滤,
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及流程中的分离方法为解答的关键,侧重分析与实验能力的考查,注意溶解度的应用,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
17.已知下列三种气态物质之间的反应:
C2H2(g)+H2(g)?C2H4(g) ①
2CH4(g)?C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g);△H=-Q1 kJ/mol
C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g);△H=-Q2 kJ/mol
C(s)+H2(g)=$\frac{1}{2}$C2H4(g);△H=-Q3 kJ/mol
Q1、Q2、Q3均为正值,下列关系正确的是( )
C2H2(g)+H2(g)?C2H4(g) ①
2CH4(g)?C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g);△H=-Q1 kJ/mol
C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g);△H=-Q2 kJ/mol
C(s)+H2(g)=$\frac{1}{2}$C2H4(g);△H=-Q3 kJ/mol
Q1、Q2、Q3均为正值,下列关系正确的是( )
| A. | Q1>Q3>Q2 | B. | Q1>Q2>Q3 | C. | Q2>Q1>Q3 | D. | Q3>Q1>Q2 |
14.生物硝化法处理含NH4+的废水的原理如图所示(不考虑其他物质影响),下列说法不正确的是( )

| A. | 可用NaOH和湿润的红色的石蕊试纸检验NH4+ | |
| B. | 该方法会导致水体pH下降 | |
| C. | 该方法中O2做氧化剂,微生物做还原剂 | |
| D. | 处理后的废水需进一步处理才能排放 |
1.某有机化合物结构简式如图,下列有关它的性质的叙述中,正确的是( )


| A. | 有弱酸性,与Na2CO3、NaHCO3溶液均能反应 | |
| B. | 在一定条件下,1 mol该物质最多能与3 mol NaOH完全反应 | |
| C. | 在一定条件下,该物质可以发生取代、加成、水解、消去反应 | |
| D. | 该有机物分子中所有碳原子可能共平面 |
11.某同学为配置含有X,SO42-,Mg2+,NO3-四种离子的无色溶液,要使四种离子的物质的量浓度之比为1:2:1:1,则X应该是:( )
| A. | Fe3+ | B. | Al3+ | C. | NH4+ | D. | Cl- |
18.工业上用铝土矿(主要成分为Al203,含Fe2O3等杂质)为原料冶炼铝的工艺流程如图:对上述流程中的判断正确的是( )
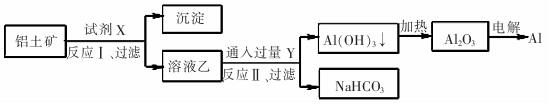

| A. | 试剂X为稀硫酸 | |
| B. | 反应Ⅱ中生成Al(OH)3的反应为:CO2+AlO2-+2H20=Al(OH)3↓+HCO3一 | |
| C. | 结合质子( H+)的能力由强到弱的顺序是Al02->CO32->OH- | |
| D. | Al2O3熔点很高,工业上还可采用电解熔融AICl3冶炼Al |
16.为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4.为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
(1)测定过程中有关反应的离子方程式为H++OH-=H2O、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为0.84L.
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比.
(4)欲计算该NaOH溶液的物质的量浓度应选择第Ⅲ组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程.
| 实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
| Ⅰ | 7.4 | 40.00 | 1.68 |
| Ⅱ | 14.8 | 40.00 | 3.36 |
| Ⅲ | 22.2 | 40.00 | 1.12 |
| Ⅳ | 37.0 | 40.00 | 0 |
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为0.84L.
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比.
(4)欲计算该NaOH溶液的物质的量浓度应选择第Ⅲ组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程.
 ;Al与NaOH溶液反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
;Al与NaOH溶液反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.