题目内容
下列有关实验原理或实验操作不正确的是( )
A、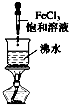 实验室制备氢氧化铁胶体 |
B、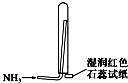 氨气的收集、检验装置 |
C、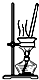 蒸发结晶获得胆矾晶体 |
D、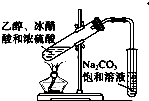 实验室制乙酸乙酯 |
考点:化学实验方案的评价
专题:
分析:A.在沸水中滴加饱和氯化铁溶液制备氢氧化铁胶体;
B.氨气密度比空气小,可使湿润的红色石蕊试纸变蓝色;
C.可利用蒸发、浓缩的方法制备晶体;
D.注意防止倒吸.
B.氨气密度比空气小,可使湿润的红色石蕊试纸变蓝色;
C.可利用蒸发、浓缩的方法制备晶体;
D.注意防止倒吸.
解答:
解:A.在沸水中滴加饱和氯化铁溶液制备氢氧化铁胶体,注意当溶液变成红褐色时停止加热,故A正确;
B.氨气密度比空气小,可使湿润的红色石蕊试纸变蓝色,可完成实验,故B正确;
C.可利用蒸发、浓缩、冷却结晶的方法制备胆矾晶体,故C正确;
D.导管不能插入液面以下,防止倒吸,故D错误.
故选D.
B.氨气密度比空气小,可使湿润的红色石蕊试纸变蓝色,可完成实验,故B正确;
C.可利用蒸发、浓缩、冷却结晶的方法制备胆矾晶体,故C正确;
D.导管不能插入液面以下,防止倒吸,故D错误.
故选D.
点评:本题考查较为综合,涉及物质的制备、检验以及分离等,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
二氧化硅晶体是立体的网状结构,其结构如图所示.关于二氧化硅晶体的下列说法不正确的是( )
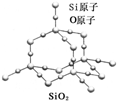

| A、晶体中Si、O原子个数比为1:2 |
| B、晶体中Si、O原子最外层都满足8电子结构 |
| C、晶体中一个硅原子含有Si-O键数目为4 |
| D、晶体中最小环上的原子数为6 |
铝能用于冶炼难熔的金属,这是因为铝具有( )
| A、两性 |
| B、优良的导电性 |
| C、低的熔点 |
| D、还原性,且在冶炼反应中放出大量热 |