题目内容
如图所示,反应:X(气)+3Y(气)═2Z(气);△H<0,在不同温度、不同压强下(p1>p2),达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )
A、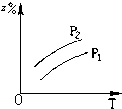 |
B、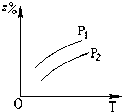 |
C、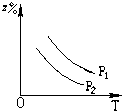 |
D、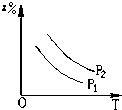 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由方程式X(气)+3Y(气) 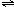 2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,
2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,
反应前气体的化学计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,以此判断生成物Z的百分含量的变化.
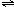 2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,
2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,反应前气体的化学计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,以此判断生成物Z的百分含量的变化.
解答:
解:由方程式X(气)+3Y(气) 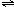 2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,则生成物Z的百分含量减小,可排除A、B选项;
2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,则生成物Z的百分含量减小,可排除A、B选项;
反应前气体的化学计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,则生成物Z的百分含量增大,又P1>P2,则C正确,D错误.
故选C.
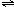 2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,则生成物Z的百分含量减小,可排除A、B选项;
2Z(气)+热量,可知:反应放热,升高温度平衡向逆反应方向移动,则生成物Z的百分含量减小,可排除A、B选项;反应前气体的化学计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,则生成物Z的百分含量增大,又P1>P2,则C正确,D错误.
故选C.
点评:本题考查化学平衡移动图象问题,题目难度不大,注意从化学方程式的反应热以及化学计量数关系判断外界条件对平衡移动的影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关实验原理或实验操作不正确的是( )
A、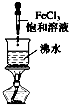 实验室制备氢氧化铁胶体 |
B、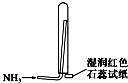 氨气的收集、检验装置 |
C、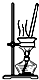 蒸发结晶获得胆矾晶体 |
D、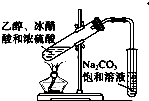 实验室制乙酸乙酯 |
在铁的氧化物和氧化铝组成的混合物中,加入2mol/L硫酸溶液65mL,恰好完全反应.所得溶液中Fe2+能被标准状况下112mL氯气氧化.则原混合物中金属元素和氧元素的原子个数之比为( )
| A、5:7 | B、4:3 |
| C、3:4 | D、9:13 |
镁粉在焰火、闪光粉中是不可少的原料,工业制造镁粉的最后一步是将镁蒸气在气体中冷却,下列可作为冷却气体的是( )
| A、空气 |
| B、O2 |
| C、CO2 |
| D、H2 |
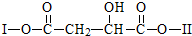 (其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化:
(其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化: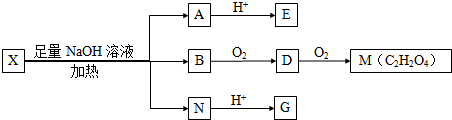
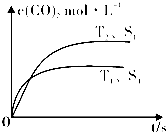 2014年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2014年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.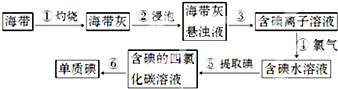
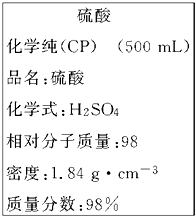 如图是我校实验室化学试剂浓硫酸标签上的部分内容.现需要480mL 1mol?L-1的稀硫酸.用该浓硫酸和蒸馏水配制,可供选用的仪器有:
如图是我校实验室化学试剂浓硫酸标签上的部分内容.现需要480mL 1mol?L-1的稀硫酸.用该浓硫酸和蒸馏水配制,可供选用的仪器有: