��Ŀ����
��100��ʱ����0.5mol N2O4ͨ�����Ϊ5L������ܱ������У��������ֺ���ɫ����Ӧ���е�2sʱ��NO2��Ũ��Ϊ0.02mol/L����60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6��������˵����ȷ���ǣ�������
| A��ǰ2s��N2O4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.01mol/��L?s�� |
| B����2sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1�� |
| C����ƽ��ʱ��ϵ�ں�N2O4 0.25mol |
| D��ƽ��ʱ��N2O4��ת����Ϊ40% |
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
������2��ʱ��NO2��Ũ��Ϊ0.02Ħ/������ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ�ٶȣ�
���ݻ�ѧƽ������ʽ��ʽ���㣬��Ӧ���е�60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6����������N2O4�����ʵ���Ϊx����ʽ����
N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� x 2x
ƽ������mol��0.5-x 2x
0.5-x+2x=0.5��1.6
x=0.3mol��
���ݻ�ѧƽ������ʽ��ʽ���㣬��Ӧ���е�60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6����������N2O4�����ʵ���Ϊx����ʽ����
N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� x 2x
ƽ������mol��0.5-x 2x
0.5-x+2x=0.5��1.6
x=0.3mol��
���
�⣺2��ʱ��NO2��Ũ��Ϊ0.02Ħ/������ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ�ٶȣ�
��Ӧ���е�60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6����������N2O4�����ʵ���Ϊx����
N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� x 2x
ƽ������mol��0.5-x 2x
0.5-x+2x=0.5��1.6
x=0.3mol��
A��2��ʱ��NO2��Ũ��Ϊ0.02Ħ/������ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��ʾ��ƽ����Ӧ�ٶ�Ϊ
=0.005mol/��L��s������A����
B��N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� 0.05 0.1
ƽ������mol�� 0.45 0.1
ѹǿ��ϵ2sʱ��ϵ�ڵ�ѹǿ����ʼѹǿ=0.55��0.5=1.1��1����2sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1������B��ȷ��
C����ƽ��ʱ��ϵ�ں�N2O4=0.5mol-0.3mol=0.2mol����C����
D��ƽ��ʱ��N2O4��ת����=
��100%=60%����D����
��ѡB��
��Ӧ���е�60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6����������N2O4�����ʵ���Ϊx����
N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� x 2x
ƽ������mol��0.5-x 2x
0.5-x+2x=0.5��1.6
x=0.3mol��
A��2��ʱ��NO2��Ũ��Ϊ0.02Ħ/������ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��ʾ��ƽ����Ӧ�ٶ�Ϊ
| 0.01mol/L |
| 2s |
B��N2O4�T2NO2��
��ʼ����mol�� 0.5 0
�仯����mol�� 0.05 0.1
ƽ������mol�� 0.45 0.1
ѹǿ��ϵ2sʱ��ϵ�ڵ�ѹǿ����ʼѹǿ=0.55��0.5=1.1��1����2sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1������B��ȷ��
C����ƽ��ʱ��ϵ�ں�N2O4=0.5mol-0.3mol=0.2mol����C����
D��ƽ��ʱ��N2O4��ת����=
| 0.3mol |
| 0.5mol |
��ѡB��
���������⿼�黯ѧƽ�⼰��ѧ��Ӧ���ʵļ��㣬��Ŀ�Ѷ��еȣ���ȷ��Ϣ�е�ѹǿ��ϵ����ͬʱ������ϵ�и����ʵ����ʵ����Ĺ�ϵ�ǽ��Ĺؼ�������Ϥ��ѧ��Ӧ���ʵļ���ʽ��Ӱ�컯ѧƽ���ƶ������ؼ��ɽ��

��ϰ��ϵ�д�
 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
�����Ŀ
CH4��H2�������10mL����ȫȼ�պ�����6mL CO2���壨��������Ϊ��ͬ״���²ⶨ��������������CH4��H2�������Ϊ��������
| A��2��3 | B��3��2 |
| C��2��1 | D��1��2 |
���з�Ӧ������ʵ�����Ʊ��������ǣ�������
�ٸ�������ȷֽ⣺2KMnO4�TK2MnO2+MnO2+O2������������ȷֽ� 2NH4NO3
2N2��+O2��+4H2O���۹���������ˮ��Ӧ 2Na2O2+2H2O�T4NaOH+O2�����ܶ��������ȷֽ� 2NO2
2NO+O2��
�ٸ�������ȷֽ⣺2KMnO4�TK2MnO2+MnO2+O2������������ȷֽ� 2NH4NO3
| ||
| ||
| A���� | B���ٺ͢� |
| C���ٺ͢� | D���٢ۢ� |
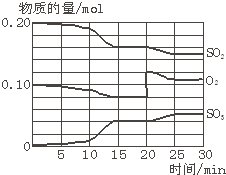
���淴Ӧ��X��g��+2Y��g��?2Z��g������2M��g��?N��g��+P��g���ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���壮��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ�������ж���ȷ���ǣ�������


| A����Ӧ�ٵ��淴Ӧ�Ƿ��ȷ�Ӧ | ||
| B����ƽ�⣨��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ11��10 | ||
C����ƽ�⣨��ʱ��X��ת����Ϊ
| ||
| D����ƽ�⣨��ƽ�⣨���У�M������������ |
��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±�����˵��������ǣ�������
| ���� | X | Y | Z |
| ��ʼŨ��/mol?L-1 | 0.1 | 0.2 | 0 |
| ƽ��Ũ��/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A����Ӧ�ﵽƽ��ʱ��y��ת����Ϊ75% |
| B����Ӧ�ɱ�ʾΪX+3Y?2Z����ƽ�ⳣ��Ϊ1600 |
| C������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������ |
| D���ı��¶ȵ������Ըı�˷�Ӧ��ƽ�ⳣ�� |
Wg����Fe2O3?xH2O���ʵ�Al2O3��Ʒ����ȫ�ܽ���100mL c��H+��=0.1mol/L��ϡH2SO4�У�Ȼ������Һ�м���100mL��ˮ��ǡ�õõ��ij������������N g�������Ӱ�ˮ��Ũ���ǣ�������
| A��0.05 mol?L-1 |
| B��0.1 mol?L-1 |
| C��0.15 mol?L-1 |
| D��0.2 mol?L-1 |
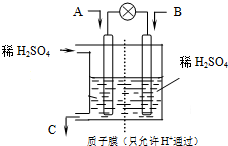 ���ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ���⣮
���ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ���⣮