题目内容
可逆反应①X(g)+2Y(g)?2Z(g)、②2M(g)?N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板.反应开始和达到平衡状态时有关物理量的变化如图所示:下列判断正确的是( )


| A、反应①的逆反应是放热反应 | ||
| B、达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为11:10 | ||
C、达平衡(Ⅰ)时,X的转化率为
| ||
| D、在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等 |
考点:化学平衡的计算
专题:化学平衡专题
分析:A、从降温导致平衡(Ⅰ)向平衡(Ⅱ)移动时,X、Y、Z的总物质的量变化导致反应移动的方向来判断反应是吸热还是放热;
B、根据等温时,反应②中气体的物质的量不变,压强与体积成反比,并且左右两个容器中的压强关系可判断;
C、相同压强下,根据物质的量之比等于体积之比计算①中气体的物质的量,进而求出转化率;
D、由于温度变化反应②的平衡已经被破坏,M的体积分数不会相等的.
B、根据等温时,反应②中气体的物质的量不变,压强与体积成反比,并且左右两个容器中的压强关系可判断;
C、相同压强下,根据物质的量之比等于体积之比计算①中气体的物质的量,进而求出转化率;
D、由于温度变化反应②的平衡已经被破坏,M的体积分数不会相等的.
解答:
解:A、降温由平衡(Ⅰ)向平衡(Ⅱ)移动,同时X、Y、Z的总物质的量减少,说明平衡向右移动,正反应放热,逆反应为吸热反应,故A错误;
B、平衡时,右边物质的量不变,由图可以看出达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为:
=
,故B错误;
C、达平衡(Ⅰ)时,右边气体的物质的量不变,仍为2mol,左右气体压强相等,设平衡时左边气体的物质的量为xmol,
则有:
=
,x=
=
mol,即物质的量减少了3-
=
mol,所以达平衡(Ⅰ)时,X的转化率为
;故C正确;
D、由平衡(Ⅰ)到平衡(Ⅱ),化学反应②发生移动,M的体积分数不会相等的,故D错误.
故选:C.
B、平衡时,右边物质的量不变,由图可以看出达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为:
| 2 |
| 2.2 |
| 10 |
| 11 |
C、达平衡(Ⅰ)时,右边气体的物质的量不变,仍为2mol,左右气体压强相等,设平衡时左边气体的物质的量为xmol,
则有:
| 2 |
| x |
| 2.2 |
| 2.8 |
| 2×2.8 |
| 2.2 |
| 28 |
| 11 |
| 28 |
| 11 |
| 5 |
| 11 |
| 5 |
| 11 |
D、由平衡(Ⅰ)到平衡(Ⅱ),化学反应②发生移动,M的体积分数不会相等的,故D错误.
故选:C.
点评:本题考查化学平衡移动问题,具有一定难度,做题注意从右边反应体系中的物质的量不变考虑.

练习册系列答案
相关题目
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量水能使溶液恢复到电解前的浓度的是( )
| A、AgNO3 |
| B、Na2SO4 |
| C、CuCl2 |
| D、HCl |
实验室常用饱和的NaNO2与NH4Cl溶液反应制取少量的氮气.反应的化学方程式如下:NaNO2+NH4Cl
NaCl+N2↑+2H2O,则氮气的发生装置与下列气体中发生装置相同的是( )
| ||
| A、H2 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
将1.0mol PCl3,和1.0mol Cl2充入体积不变的1L密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g)达到平衡时,PCl5为0.50mol,如果此时将PCl3和Cl2全部移走,在相同温度下再达平衡时PCl5的物质的量是( )
| A、0.50mol |
| B、0.19mol |
| C、0.25mol |
| D、0.31mol |
在100℃时,把0.5mol N2O4通入体积为5L的真空密闭容器中,立即出现红棕色.反应进行到2s时,NO2的浓度为0.02mol/L.在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍.下列说法正确的是( )
| A、前2s以N2O4的浓度变化表示的反应速率为0.01mol/(L?s) |
| B、在2s时体系内的压强为开始时的1.1倍 |
| C、在平衡时体系内含N2O4 0.25mol |
| D、平衡时,N2O4的转化率为40% |
分析如下残缺的反应:RO3-+ +6H+=3R2↑+3H2O.下列叙述正确的是( )
| A、上式中缺项所填物质在反应中作氧化剂 | ||
| B、R的原子半径在同周期元素原子中最小 | ||
| C、R一定是周期表中的第VA族元素 | ||
D、RO
|
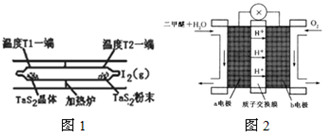
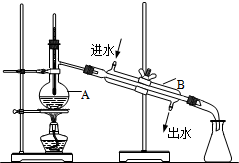 如图为实验室制取自来水的装置示意图,根据图示回答下列问题.
如图为实验室制取自来水的装置示意图,根据图示回答下列问题.