题目内容
8.下列说法不合理的是( )| A. | 全球气候变暖可能是由于二氧化碳含量的急剧增加 | |
| B. | 酸雨可以分为硫酸型酸雨和硝酸型酸雨 | |
| C. | 居室中的装潢材料缓慢释放出来的污染物中最常见的是甲醛、苯等有机物蒸气 | |
| D. | 检验居室中甲醛气体是否存在,可以抽取并通过品红溶液来检验 |
分析 A.二氧化碳可导致温室效应;
B.二氧化硫、氮氧化物可导致酸雨;
C.甲醛、苯等常用于装饰材料的溶剂和防腐剂;
D.甲醛与品红不反应.
解答 解:A.二氧化碳为导致温室效应的主要气体,可导致全球气候变暖,故A正确;
B.二氧化硫、氮氧化物溶于水,与水反应生成亚硫酸、硫酸、硝酸,可导致酸雨,故B正确;
C.甲醛、苯等常用于装饰材料的溶剂和防腐剂,二者对人体有害,为致癌物质,为装饰材料的主要污染物质,故C正确;
D.甲醛与品红不反应,不能用品红检验甲醛,故D错误.
故选D.
点评 本题考查常见生活环境的污染,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,题目难度不大,注意常见物质的应用和性质,注重相关基础知识的积累.

练习册系列答案
相关题目
20.将4g NaOH溶于36g水中,可使溶液中H2O与Na+的物质的量之比为20:1,此溶液中溶质的质量分数为10%.若测得该溶液的密度为1.1g/cm3,则溶液中c(Na+)为2.75mol/L.
3.下列叙述中正确的是( )
| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 含氧酸可作氧化剂而无氧酸则不能 | |
| C. | 金属原子失电子数越多,其还原性越强 | |
| D. | 金属单质在反应中只作还原剂 |
13.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{还原}^{H_{2}}$Si | |
| B. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| C. | FeS2$→_{还原}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| D. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg |
17.已知在25℃,101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ/mol | |
| B. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ/mol | |
| C. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l);△;△H=+5518kJ/mol | |
| D. | 2C8H18(1)+25O2(g)=16CO2(g)+18H2O(1);△H=-11036kJ/mol |
18.将一定量氯气通入刚吸收过少量SO2的NaOH溶液,所得溶液仍显强碱性.
(1)请完成SO2与过量NaOH溶液反应的化学方程式SO2+2NaOH=Na2SO3+H2O
(2)所得溶液中一定存在的阴离子为SO42-和Cl-、OH-
(3)设计实验方案,探究所得溶液中是否含有SO32-或ClO-.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
(1)请完成SO2与过量NaOH溶液反应的化学方程式SO2+2NaOH=Na2SO3+H2O
(2)所得溶液中一定存在的阴离子为SO42-和Cl-、OH-
(3)设计实验方案,探究所得溶液中是否含有SO32-或ClO-.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量所得溶液于试管中,滴加3mol.L-1H2SO至溶液呈酸性,然后将所得溶液分置于A、B试管中 | |
| 步骤2: | |
| 步骤3: |
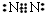 ;
;
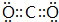
 ,用电子式表示化合物 C2D 的形成过程
,用电子式表示化合物 C2D 的形成过程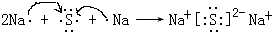 .
.