题目内容
17.已知在25℃,101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )| A. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ/mol | |
| B. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ/mol | |
| C. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l);△;△H=+5518kJ/mol | |
| D. | 2C8H18(1)+25O2(g)=16CO2(g)+18H2O(1);△H=-11036kJ/mol |
分析 在25℃时,101kPa下,1g辛烷燃烧生成二氧化碳和液态水放出48.40KJ的热量,根据m=nM计算出1mol辛烷的质量,然后计算出1mol辛烷完全燃烧放出的热量,再根据反应物和生成物的状态及反应热写出其热化学反应方程式.
解答 解:1mol辛烷的质量为:114g/mol×1mol=114g,25℃时,101kPa下,1g辛烷燃烧生成二氧化碳和液态水放出48.40KJ的热量,则1mol辛烷(114g)燃烧生成二氧化碳和液态水放出热量为:48.40kJ×$\frac{114g}{1g}$=5518kJ,
所以C8H18燃烧的热化学反应方程式为:C8H18(l)+12.5O2(g)=8CO2(g)+9H2O(l)△H=-5518kJ/mol,
故选B.
点评 本题考查了热化学反应方程式的书写,题目难度不大,注意物质的聚集状态和对应化学方程式计量数的反应焓变计算,试题侧重基础知识的考查,有利于培养学生的分析能力及灵活应用能力.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
7.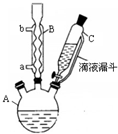 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图:
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图:
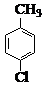 $→_{催化剂}^{KMnO_{4}}$
$→_{催化剂}^{KMnO_{4}}$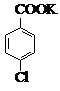 +MnO2
+MnO2
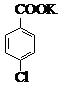
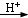
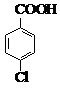
常温条件下的有关数据如下表所示:
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g.
请回答下列问题:
(1)装置B的名称是冷凝管.
(2)量取6.00mL对氯甲苯应选用的仪器是C.
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是水浴加热.对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是减少对氯甲苯的挥发,提高原料利用率.
(4)第一次过滤的目的是除去MnO2,滤液中加入稀硫酸酸化,可观察到的实验现象是产生白色沉淀.
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是可除去对氯苯甲酸表面的可溶性杂质且尽量减小对氯苯甲酸的损耗.
(6)本实验的产率是D(填标号).
A.60% B.70% C.80% D.90%
 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图:
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图: $→_{催化剂}^{KMnO_{4}}$
$→_{催化剂}^{KMnO_{4}}$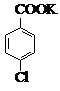 +MnO2
+MnO2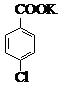
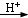
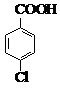
常温条件下的有关数据如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
请回答下列问题:
(1)装置B的名称是冷凝管.
(2)量取6.00mL对氯甲苯应选用的仪器是C.
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是水浴加热.对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是减少对氯甲苯的挥发,提高原料利用率.
(4)第一次过滤的目的是除去MnO2,滤液中加入稀硫酸酸化,可观察到的实验现象是产生白色沉淀.
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是可除去对氯苯甲酸表面的可溶性杂质且尽量减小对氯苯甲酸的损耗.
(6)本实验的产率是D(填标号).
A.60% B.70% C.80% D.90%
8.下列说法不合理的是( )
| A. | 全球气候变暖可能是由于二氧化碳含量的急剧增加 | |
| B. | 酸雨可以分为硫酸型酸雨和硝酸型酸雨 | |
| C. | 居室中的装潢材料缓慢释放出来的污染物中最常见的是甲醛、苯等有机物蒸气 | |
| D. | 检验居室中甲醛气体是否存在,可以抽取并通过品红溶液来检验 |
5.CoCl2•6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如下:
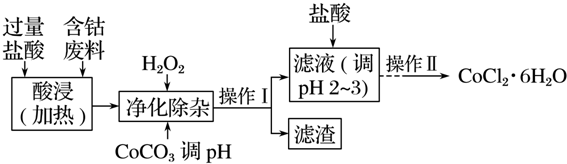
已知:
(1)净化除杂质时,加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.

已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.
12.下列三种烃的立体结构如图示:
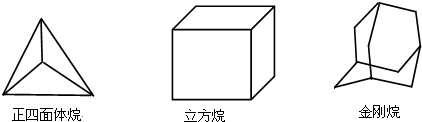
则这三种烃的二氯取代产物的同分异构体数目分别是( )

则这三种烃的二氯取代产物的同分异构体数目分别是( )
| A. | 2,4,8 | B. | 2,4,6 | C. | 1,3,6 | D. | 1,3,8 |
2.体积为V mL、密度为ρg/cm3的溶液中,含相对分子质量为M的溶质m g,物质的量浓度为c mol/L,溶质质量分数为W%.下列表示式中正确的是( )
| A. | c=$\frac{m}{VM}$ | B. | m=ρVM | C. | W%=$\frac{cM}{1000p}$% | D. | c=$\frac{1000ρW%}{M}$ |
6.节能减排是社会赋予的责任和使命,从衣、食、住、行、用等方面,下列行为不利于低碳生活的是( )
①用LED半导体节能照明灯代替传统的白炽灯
②购物时提倡用超薄一次性塑料袋
③推广使用一次性筷子
④在农村推广沼气照明和供热
⑤用大排量的轿车代替公交车出行.
①用LED半导体节能照明灯代替传统的白炽灯
②购物时提倡用超薄一次性塑料袋
③推广使用一次性筷子
④在农村推广沼气照明和供热
⑤用大排量的轿车代替公交车出行.
| A. | ③④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①②⑤ |
7.下列反应或变化中属于放热反应的是( )
| A. | C+CO2 $\frac{\underline{\;加热\;}}{\;}$2CO | B. | 2H2+O2 $\frac{\underline{\;高温\;}}{\;}$2H2O | ||
| C. | CaCO3 $\frac{\underline{\;点燃\;}}{\;}$ CaO+CO2 | D. | 水蒸汽凝结成水 |

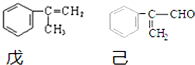
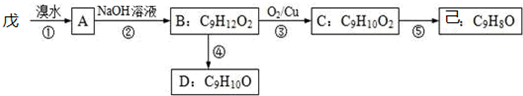
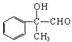
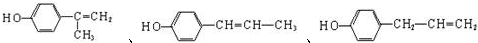 .
. .
.