题目内容
13.在给定的条件下,下列选项所示的物质间转化均能实现的是( )| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{还原}^{H_{2}}$Si | |
| B. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| C. | FeS2$→_{还原}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| D. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg |
分析 A.二氧化硅为酸性氧化物和盐酸不反应;
B.氮气和氢气一定条件下反应生成氨气,氨气和盐酸反应生成氯化铵;
C.FeS2燃烧生成二氧化硫,二氧化硫和水反应生成亚硫酸;
D.碳酸镁和盐酸反应生成氯化镁、二氧化碳和水,氯化镁溶液电解不能生成金属镁.
解答 解:A.二氧化硅属于酸性氧化物和盐酸不反应,不能一步实现反应,故A错误;
B.氮气和氢气在催化剂、高温高压条件下反应生成氨气,氨气是碱性气体和盐酸反应生成氯化铵,两步反应能一步实现,故B正确;
C.FeS2燃烧生成二氧化硫,不能生成三氧化硫,故C错误;
D.碳酸镁溶于盐酸生成氯化镁溶液,氯化镁溶液电解得到氢氧化镁,氢气和氯气,不能直接得到金属镁,应是电解熔融状态的氯化镁得到金属镁,故D错误;
故选B.
点评 本题考查了物质性质、物质转化的应用,为高频考点,侧重学生的分析能力的考查,主要是硅、硫、氮、镁的化合物性质的理解判断,注意相关基础知识的积累,题目较简单.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
5.对下列各组物质的分类正确的是( )
①混合物:水玻璃、水银、水煤气
②电解质:明矾、冰醋酸、石膏
③酸性氧化物:CO2、Al2O3、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C60、金刚石、石墨
⑥干冰、液氯都是非电解质.
①混合物:水玻璃、水银、水煤气
②电解质:明矾、冰醋酸、石膏
③酸性氧化物:CO2、Al2O3、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C60、金刚石、石墨
⑥干冰、液氯都是非电解质.
| A. | ①②③④⑤⑥ | B. | ④⑥ | C. | ②⑤⑥ | D. | ②⑤ |
4.为除去某物质中所含的杂质,周佳敏同学做了以下四组实验,其中她所选用的试剂或操作方法正确的是( )
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| ③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
8.下列说法不合理的是( )
| A. | 全球气候变暖可能是由于二氧化碳含量的急剧增加 | |
| B. | 酸雨可以分为硫酸型酸雨和硝酸型酸雨 | |
| C. | 居室中的装潢材料缓慢释放出来的污染物中最常见的是甲醛、苯等有机物蒸气 | |
| D. | 检验居室中甲醛气体是否存在,可以抽取并通过品红溶液来检验 |
18.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm).
(1)C元素在元素周期表中的位置是第三周期第Ш A族;
(2)B的原子结构示意图为 ;
;
(3)D、E气态氢化物的稳定性强弱顺序为H2S<HCl(填化学式);
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是HClO4(填化学式);
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:ACD;
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
(7)液态GA3的电离方式与液态A2F类似,则液态GA3的电离方程式为2NH3(l) NH4++NH2-.
NH4++NH2-.
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.037 | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | -1 | -2 | +5、-3 |
(2)B的原子结构示意图为
 ;
;(3)D、E气态氢化物的稳定性强弱顺序为H2S<HCl(填化学式);
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是HClO4(填化学式);
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:ACD;
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
(7)液态GA3的电离方式与液态A2F类似,则液态GA3的电离方程式为2NH3(l)
 NH4++NH2-.
NH4++NH2-.
5.CoCl2•6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如下:
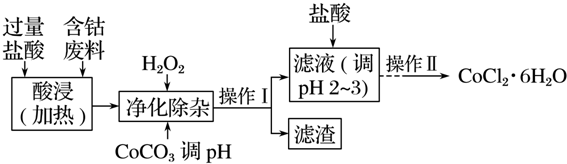
已知:
(1)净化除杂质时,加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.

已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.
2.体积为V mL、密度为ρg/cm3的溶液中,含相对分子质量为M的溶质m g,物质的量浓度为c mol/L,溶质质量分数为W%.下列表示式中正确的是( )
| A. | c=$\frac{m}{VM}$ | B. | m=ρVM | C. | W%=$\frac{cM}{1000p}$% | D. | c=$\frac{1000ρW%}{M}$ |
3.进行化学实验必须注意安全,下列说法正确的是( )
| A. | 不慎将酸溅到眼中,应立即用干布擦,后边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 酒精在实验台上燃烧时,用水扑灭火焰 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
 ;AB2的结构式是O=C=O.
;AB2的结构式是O=C=O.