题目内容
9.下列有关表述错误的是( )| A. | IBr的电子式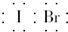 | B. | HClO的结构式为H-O-Cl | ||
| C. | HIO各原子都满足8电子结构 | D. | NaBr的形成过程可以表示为: |
分析 A.IBr为共价化合物,分子中含有1个I-Br键;
B.次氯酸中含有1个氢氧键和1个O-Cl键;
C.HIO分子中,H原子最外层电子数为2;
D.溴化钠为离子化合物,电子式中阴阳离子都需要标出所带电荷,溴离子还需要标出最外层电子.
解答 解:A.IBr为共价化合物,I、Br原子之间形成的一对共用电子对,其电子式为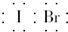 ,故A正确;
,故A正确;
B.HClO的中心原子为O,其结构式为:H-O-Cl,故B正确;
C.HIO中I、O原子最外层满足8电子稳定结构,而H原子最外层电子数为2,故C错误;
D.溴化银为离子化合物,用电子式表示溴化钠的形成过程为: ,故D正确;
,故D正确;
故选C.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及电子式、结构式、核外电子排布等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
14.可逆反应A(g)+B(s)?C(g)+D(g)在恒温恒容的密闭容器中进行,下列选项中不能说明该反应已经达到平衡状态的是( )
| A. | 消耗amolA物质的同时消耗amolC物质 | |
| B. | 混合气体的质量不再改变 | |
| C. | B物质的浓度不再改变 | |
| D. | 容器内的压强不再改变 |
1.制取氯乙烷(CH3-CH2Cl)的最好方法是( )
| A. | 乙烷与氯气发生取代反应 | B. | 乙烯与氯气发生加成反应 | ||
| C. | 乙烯与氯化氢发生加成反应 | D. | 甲烷与氯气发生取代反应 |
18.设NA为阿伏加德罗常数的值,则下列说法正确的是( )
| A. | 标准状况下,2.24L CCl4中含有的分子数为0.1NA | |
| B. | 常温常压下,46 g NO2气体中含有原子数为3NA | |
| C. | 18 g重水(D2O)中含有的电子数为10NA | |
| D. | 1 molNa2O2与足量水蒸气反应转移电子总数为2NA |
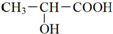 .在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题:
.在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题: 木糖的分子式为C5H10O5,属于多羟基醛,木糖在浓硫酸作用下生成糠醛(结构简式如图).
木糖的分子式为C5H10O5,属于多羟基醛,木糖在浓硫酸作用下生成糠醛(结构简式如图). .
. ,回答下列问题:
,回答下列问题: (间、对位也可以).
(间、对位也可以).
 .写出反应③的化学方程式
.写出反应③的化学方程式 .①的反应类型为取代反应.
.①的反应类型为取代反应. →□→□$\stackrel{(连续氧化)}{→}$□→
→□→□$\stackrel{(连续氧化)}{→}$□→
 $→_{Zn、H_{2}O}^{O_{3}}$R1CHO+
$→_{Zn、H_{2}O}^{O_{3}}$R1CHO+
 +HCl.
+HCl. ,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.