题目内容
18.设NA为阿伏加德罗常数的值,则下列说法正确的是( )| A. | 标准状况下,2.24L CCl4中含有的分子数为0.1NA | |
| B. | 常温常压下,46 g NO2气体中含有原子数为3NA | |
| C. | 18 g重水(D2O)中含有的电子数为10NA | |
| D. | 1 molNa2O2与足量水蒸气反应转移电子总数为2NA |
分析 A.气体摩尔体积适用对象为气体;
B.根据二氧化氮的质量计算出原子的物质的量及数目;
C.依据n=$\frac{m}{M}$计算物质的量,结合分子结构计算电子数;
D.过氧化钠和水反应方程式为2Na2O2+2H2O=4NaOH+O2↑,该反应过氧化钠中O元素化合价由-1价变为-2价和0价;
解答 解:A.标准状况下,CCl4为液体,不能使用气体摩尔体积,故A错误;
B.46gNO2的物质的量是1mol,含有3mol原子,含有原子数为3NA,故B正确;
C.依据n=$\frac{m}{M}$计算物质的量=$\frac{18g}{20g/mol}$=0.9mol,结合分子结构计算电子数为9NA,故C错误;
D.1mol过氧化钠和水反应转移电子数=1mol×1×NA/mol=NA,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的分析判断,主要是物质的量和物理量的计算,气体摩尔体积的条件应用,氧化还原反应分析理解是解题关键,题目较简单.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
9.下列有关表述错误的是( )
| A. | IBr的电子式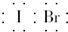 | B. | HClO的结构式为H-O-Cl | ||
| C. | HIO各原子都满足8电子结构 | D. | NaBr的形成过程可以表示为: |
13.下列说法正确的是( )
| A. | 质谱法是检测分子的结构,红外光谱法是测定有机物的相对分子质量 | |
| B. | 汽油燃烧的汽车尾气中,所含的大气污染物主要是碳的氧化物、氮的氧化物、硫的氧化物和水 | |
| C. | 组成为C3H6Cl2的卤代烷烃存在4种同分异构体 | |
| D. | 乙酸乙酯在酸性和碱性条件下都可以发生水解反应,都是可逆反应 |
10.下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:通入酸性高锰酸钾溶液中;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
①除去乙烷中少量的乙烯:通入酸性高锰酸钾溶液中;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
| A. | 全部正确 | B. | ①② | C. | ②③ | D. | ③ |
7.下列说法正确的是( )
| A. | 聚氯乙烯的单体是CH2═CHCl | |
| B. | 聚乙烯的链节是CH2═CH2 | |
| C. | 通过加聚反应得到的聚乙烯属于天然高分子化合物 | |
| D. | 聚乙烯的产量是衡量一个国家石油化工发展水平的标志 |
8.将下列物质按酸、碱、盐、电解质分类排列,正确的是( )
| A. | 硝酸、纯碱、胆矾、铜 | B. | 硫酸、烧碱、小苏打、纯碱 | ||
| C. | 盐酸、乙醇、氯化钠、碘酒 | D. | 醋酸、漂白粉、石灰石、二氧化碳 |
 .
.
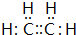 .
.