题目内容
8.下列各项中表达正确的是( )| A. | H、D、T表示同一种核素 | B. | F-离子结构示意图 | ||
| C. | 次氯酸电子式 | D. | 用电子式表示HCl形成过程 |
分析 A、具有一定质子数和中子数的原子就是一种核素;
B、氟离子的核内有9个质子,最外层有8个电子;
C、次氯酸中不存在氢氯键,其分子中存在1个氧氢键和1个氧氯键;
D、HCl是共价化合物.
解答 解:A、H、D、T为氢元素的3种不同核素,它们之间互为同位素,故A错误;
B、氟离子的核内有9个质子,最外层有8个电子,故氟离子的电子式为 ,故B正确;
,故B正确;
C、次氯酸为共价化合物,分子中不存在氢氯键,次氯酸的电子式为: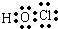 ,故C错误;
,故C错误;
D、HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程可写为: ,故D错误.
,故D错误.
故选B.
点评 本题考查电子式书写和用电子式表示化合物的形成过程,难度不大,应判断化学式中,原子间的化学键类型,再用电子式写出其形成过程.

练习册系列答案
相关题目
18.下列叙述中正确的是( )
| A. | 卤族元素是典型的非金属元素,因此不能与其他非金属元素反应 | |
| B. | 碱金属元素单质越活泼,其熔点和沸点就越高 | |
| C. | 卤族元素单质都能和氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强 | |
| D. | 卤族元素单质都能与水剧烈反应 |
3.现有部分短周期元素的性质与原子(或分子)结构如下表:
(1)画出元素T的原子结构示意图 ;
;
(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是cd(填序号);
a.Y单质的熔点比Z单质低b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式Na2O2,并写出该化合物与水反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素T和氢元素形成的化合物属于共价化合物,元素Z与元素T形成的化合物属于离子化合物(以上两空选填“共价化合物”或“离子化合物”).
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
 ;
;(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是cd(填序号);
a.Y单质的熔点比Z单质低b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式Na2O2,并写出该化合物与水反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素T和氢元素形成的化合物属于共价化合物,元素Z与元素T形成的化合物属于离子化合物(以上两空选填“共价化合物”或“离子化合物”).
13.实验探究题某课外实验小组为了探究锌与盐酸反应过程中的化学反应速率的变化,在100mL稀盐酸中加入足量的锌粉,标准状况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大,可能的原因是2~3 min;该反应是放热反应,温度升高,反应速率加快;.
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率为0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是AB(填编号).
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率为0.1mol/(L•min).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是AB(填编号).
17.下列对溶液叙述正确的是( )
| A. | 在中和滴定实验中,锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须经干燥或润洗后方可使用 | |
| B. | 用碱式滴定管量取25.00mL高锰酸钾溶液 | |
| C. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 | |
| D. | 25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW |
20.下列图象正确的是( )
| A. | 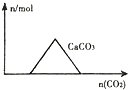 向Ca(OH)2和NaOH的混合溶液中通入CO2 | |
| B. | 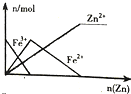 向FeCl3溶液中加入锌粉 | |
| C. |  向NaOH溶液中通入CO2 | |
| D. | 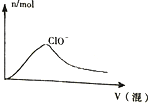 HCl与Cl2的混合通入NaOH溶液中 |
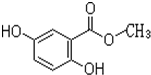 .
.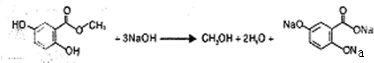 .
.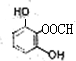 、
、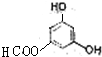 .
.
 .
. .
. .
.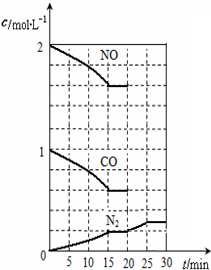 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.