题目内容
2.青蒿酸(结构如图)具有致癌抗疟作用,下列有关它的叙述不正确的是( )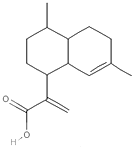
| A. | 能发生酯化反应 | B. | 属于芳香族化合物 | ||
| C. | 能与NaHCO3溶液反应 | D. | 能使溴的四氯化碳溶液褪色 |
分析 该物质中含有羧基、碳碳双键,具有羧酸和烯烃性质,能发生加成反应、加聚反应、酯化反应、取代反应等,据此分析解答.
解答 解:A.该分子中含有羧基,所以能发生酯化反应,故A正确;
B.该分子中不含苯环,所以不属于芳香族化合物,故B错误;
C.该分子中含有羧基,羧基能和碳酸氢钠反应生成羧酸钠、二氧化碳和水,故C正确;
D.该分子中含有碳碳双键,所以能和溴发生加成反应而使溴的四氯化碳溶液褪色,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查羧酸和烯烃性质,明确官能团及其性质关系是解本题关键,注意芳香族化合物中一定含有苯环,但不一定只含C、H元素,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列物质与其用途完全符合的有多少条( )
①干冰-人工降雨
②Na2CO3-制玻璃
③Fe2O3-红色油漆或涂料
④Al2O3-耐火材料
⑤NaClO-消毒剂
⑥NaCl-制纯碱;
⑦KAl (SO4 )2-消毒、净水.
①干冰-人工降雨
②Na2CO3-制玻璃
③Fe2O3-红色油漆或涂料
④Al2O3-耐火材料
⑤NaClO-消毒剂
⑥NaCl-制纯碱;
⑦KAl (SO4 )2-消毒、净水.
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
13.固体粉末X中可能含有Cu、FeO、Fe2O3、NaHCO3、Na2CO3、Na2S2O3、NaAlO2中的若干种.某化学兴趣小组为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下:
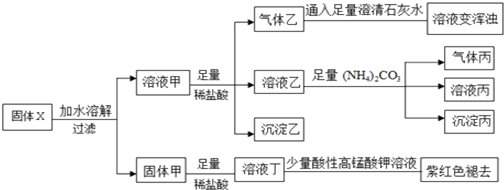
已知:HCO3-+AlO2-+H2O═Al (OH)3↓+CO32-;S2O32-+2H+═S↓+SO2↑+H2O.下列说法正确的是( )

已知:HCO3-+AlO2-+H2O═Al (OH)3↓+CO32-;S2O32-+2H+═S↓+SO2↑+H2O.下列说法正确的是( )
| A. | 气体乙和气体丙都为纯净物 | |
| B. | 固体粉末X中一定含有FeO、Na2S2O3、NaAlO2、Na2CO3,可能含有NaHCO3 | |
| C. | 溶液丁中的阳离子可能只含H+、Fe2+ | |
| D. | 溶液甲中一定含有AlO2-、CO32-、HCO3- |
17.混合气体由CH4和N2组成,测得混合气体在标准状况下的密度为0.893g/L,则混合气体中CH4和N2的体积之比为( )
| A. | 2:1 | B. | 1:4 | C. | 1:2 | D. | 4:1 |
7.下列物质中属于高分子化合物的是( )
①油脂②蔗糖③羊毛④葡萄糖⑤纤维素⑥谷氨酸⑦胃蛋白酶.
①油脂②蔗糖③羊毛④葡萄糖⑤纤维素⑥谷氨酸⑦胃蛋白酶.
| A. | ①⑤⑦ | B. | ②④⑥ | C. | ③⑤⑦ | D. | ④⑤⑥ |
14.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是BC(填序号)
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g.由此推知气体Y中SO2的体积分数为66.7%.
| 序号 | A | B | C |
| 装置 | 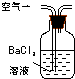 | 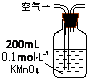 | 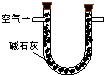 |
| 原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | lmol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 标准状况下,22.4LSO3含有NA个SO3分子 | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA | |
| D. | 56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
12.在两个烧杯中分别盛有100mL 3.0mol•L-1的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2:5,则加入的铝粉的质量为( )
| A. | 2.7 g | B. | 5.4 g | C. | 6.75 g | D. | 8.1 g |