题目内容
现有A和B的液态混合物,已知A和B的一些性质如下所示:根据图中的数据,分离A和B的液态混合物的最佳方法是( )
| 物质 | 熔点 | 沸点 | 密度 | 在水中的溶解性 |
| A | -97℃ | 86.8℃ | 0.91g/cm3 | 可溶 |
| B | -95℃ | 54.6℃ | 0.89g/cm3 | 可溶 |
| A、过滤法 | B、蒸馏法 |
| C、萃取法 | D、分液法 |
考点:物质的分离、提纯的基本方法选择与应用
专题:
分析:由表格数据可知,两种液体均溶于水,可互溶,但沸点差异较大,以此来解答.
解答:
解:由表格中数据可知A、B两物质的熔点相差不大,均易溶于水,能互溶,但是沸点相差较大,所以可以采用蒸馏的方法通过控制沸点的不同来实现二者的分离,
故选B.
故选B.
点评:本题考查混合物分离提纯方法的选择,为高频考点,把握混合物中物质的性质、性质差异为解答的关键,侧重分析与实验能力的考查,注意数据分析,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验中配制1mol?L-1的稀硫酸标准,然后用其滴定某未知浓度的氢氧化钠溶液.下列有关说法中正确的是( )
| A、实验中所用到的锥形瓶和容量瓶,在洗涤后均需要润洗 |
| B、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,最终氢氧化钠溶液浓度将偏大 |
| C、滴定时,左手提酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视滴定管内液面变化 |
| D、中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
下列说法不正确的是( )
| A、在干冰晶体中,与一个CO2分子相邻且等距离的CO2分子共有12个 |
| B、在SiO2晶体中,若含有1molSi原子,则Si-O键数为4NA |
| C、在金刚石晶体中,一个碳原子被12个六元碳环所共用,一个C-C键最多可形成6个六元环,一个六元环实际拥有一个碳原子 |
| D、mg石墨中,正六边形数目为m NA/24,每个环拥有碳原子数与C-C键数之比为2:3 |
现有一定量的Cu和Fe2O3组成的混合物,平均分成两等分,向其中一份加入2mol?L-1的盐酸溶液150mL,恰好完全溶解,所得溶液加入KSCN无血红色出现.若用过量的CO在高温下还原原混合物,固体质量减少为( )
| A、1.6 g |
| B、2.4 g |
| C、3.2 g |
| D、4.8 g |
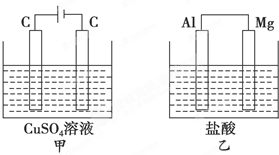 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )| A、溶液的质量变化:甲减小乙增大 |
| B、溶液pH变化:甲减小乙增大 |
| C、相同条件下产生气体的体积:V甲=V乙 |
| D、电极反应式:甲中阴极为Cu2++2e-═Cu,乙中负极为Mg-2e-═Mg2+ |
 2011年西安世园会期间对大量盆栽鲜花施用了S-诱抗素剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
2011年西安世园会期间对大量盆栽鲜花施用了S-诱抗素剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、含有碳碳双键、羧基、羟基三种官能团 |
| B、1mol该物质在催化剂加热条件下最多可与4molH2发生加成反应 |
| C、1mol该有机物与足量的溴水反应能消耗4molBr2 |
| D、该分子中所有碳原子可能位于同一平面上 |
 牙有的成分有活性物质、摩擦剂、保持牙有湿润的甘油等物质.牙宵中的摩擦剂一般由CaCO3,、Al(OH)3,SiO2中的一种或儿种物质组成.为探究某品牌牙有中摩擦剂的成分,化学兴趣小组同学做了以下实验:取适爱牙宵样品,加水充分搅拌、静置、过滤.在滤渣中加入足量盐酸后,发现仍有少铽不溶物.为进一步探究牙有中燴擦剂成分,同学们进行了以下探究:
牙有的成分有活性物质、摩擦剂、保持牙有湿润的甘油等物质.牙宵中的摩擦剂一般由CaCO3,、Al(OH)3,SiO2中的一种或儿种物质组成.为探究某品牌牙有中摩擦剂的成分,化学兴趣小组同学做了以下实验:取适爱牙宵样品,加水充分搅拌、静置、过滤.在滤渣中加入足量盐酸后,发现仍有少铽不溶物.为进一步探究牙有中燴擦剂成分,同学们进行了以下探究: 物质A~K有如图所示的转化关系(反应条件及部分产物未列出)其中A由两种元素组成,且两种元素的质量之比为7:8,B是非金属固态单质,G是金属单质,H是黄绿色气体,D为红棕色固体,C是形成酸雨的主要气体.
物质A~K有如图所示的转化关系(反应条件及部分产物未列出)其中A由两种元素组成,且两种元素的质量之比为7:8,B是非金属固态单质,G是金属单质,H是黄绿色气体,D为红棕色固体,C是形成酸雨的主要气体.