题目内容
12.下列实验一定不会出现沉淀现象的是( )| A. | CO2气体通入Na2SiO3溶液中 | B. | CO2气体通入饱和Na2CO3溶液中 | ||
| C. | SO2气体通入BaCl2溶液中 | D. | SO2气体通入Ba(OH)2溶液中 |
分析 A.CO2气体通入Na2SiO3溶液中生成硅酸沉淀;
B.饱和Na2CO3溶液中通入足量CO2反应生成碳酸氢钠,碳酸氢钠的溶解度小,因此会析出晶体,溶液变浑浊;
C.SO2溶于水生成的H2SO3是弱酸,不会与强酸的钡盐发生复分解反应;
D.SO2是酸性氧化物,少量二氧化硫通入氢氧化钡溶液生成亚硫酸钡沉淀,继续通入沉淀溶解.
解答 解:A.CO2气体通入Na2SiO3溶液中生成硅酸沉淀,有沉淀现象,故A错误;
B.饱和Na2CO3溶液中通入足量CO2反应生成碳酸氢钠,碳酸氢钠的溶解度小,因此会析出晶体,溶液变浑浊,有沉淀现象,故B错误;
C.SO2溶于水生成的H2SO3是弱酸,因为弱酸不能制强酸,SO2不能和BaCl2发生反应,所以不会出现沉淀,故C正确;
D.SO2是酸性氧化物,少量二氧化硫通入氢氧化钡溶液生成亚硫酸钡沉淀,继续通入沉淀溶解,可能有沉淀现象,故D错误.
故选C.
点评 本题考查了物质性质的应用,物质反应的产物和现象,熟练掌握物质性质是解题关键,题目难度中等.

练习册系列答案
相关题目
2.“三氯生”是一种高效广谱抗菌剂,广泛应用于牙膏、药皂、洗面奶、空气清新剂等.下面关于三氯生(C12H7Cl3O2)的说法中错误的是( )
| A. | 三氯生中含有氧气分子 | |
| B. | 三氯生由碳、氢、氯、氧四种元素组成 | |
| C. | 三氯生是一种有机物 | |
| D. | 一个三氯生分子共含有24个原子 |
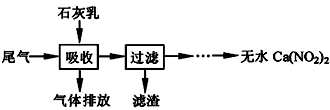

 二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂.回答下列问题:
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂.回答下列问题: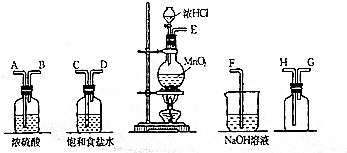
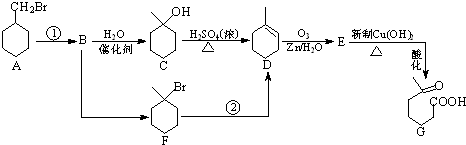
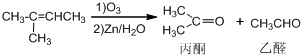
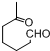 +NaOH+2Cu(OH)2$\stackrel{△}{→}$
+NaOH+2Cu(OH)2$\stackrel{△}{→}$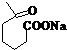 +Cu2O↓+3H2O;
+Cu2O↓+3H2O; 物质D与呋喃(
物质D与呋喃(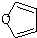 )也可以发生“Diels-Alder反应”,该化学反应方程式为
)也可以发生“Diels-Alder反应”,该化学反应方程式为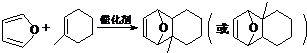 .
.