题目内容
20.一个体重50kg的健康人含铁元素2g,这2g铁元素以Fe2+和Fe3+形式存在.Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4).服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收.(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+ $?_{B}^{A}$Fe3+.在过程A中,Fe2+作还原剂;
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有还原性;
(3)某同学要检验Fe3+,向溶液中加入KSCN(写化学式)溶液变成红色.要除去FeCl3溶液中少量的氯化亚铁,可行的办法是c(填字母).
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式2Fe2++Cl2═2Fe3++2Cl?;
(4)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式2Fe3++Cu2+═2Fe2++Cu2+.
分析 (1)由Fe2+ $?_{B}^{A}$Fe3+可知,在过程A中Fe元素的化合价升高;
(2)维生素C可使食物中的Fe3+转化为Fe2+,Fe元素的化合价降低,则维生素C中某元素的化合价升高;
(3)检验Fe3+,利用KSCN溶液,除去FeCl3溶液中少量的氯化亚铁,可加入铁粉;
(4)FeCl3与金属铜反应生成氯化铜和氯化亚铁;
解答 解:(1)由Fe2+ $?_{B}^{A}$Fe3+可知,在过程A中Fe元素的化合价升高,则Fe2+为还原剂,故答案为:还原;
(2)维生素C可使食物中的Fe3+转化为Fe2+,Fe元素的化合价降低,则维生素C中某元素的化合价升高,则维生素C为还原剂,具有还原性,故答案为:还原;
(3)检验Fe3+,利用KSCN溶液,除去FeCl3溶液中少量的氯化亚铁,可加入铁粉,不会引入新的杂质,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl?,
故答案为:KSCN;c;2Fe2++Cl2═2Fe3++2Cl?;
(4)FeCl3与金属铜反应生成氯化铜和氯化亚铁,离子反应为2Fe3++Cu2+═2Fe2++Cu2+,故答案为:2Fe3++Cu2+═2Fe2++Cu2+;
点评 本题考查氧化还原反应,涉及离子检验、金属的回收、维生素C的作用等,明确反应中元素的化合价变化结合氧化还原反应即可解答,题目难度不大.

练习册系列答案
相关题目
10.下列各项中的两个量,其比值一定为2:1的是( )
| A. | 在相同温度下,等浓度的H2SO4和CH3COOH溶液中的c(H+) | |
| B. | 相同温度下,等浓度的Ba(OH)2和NaOH溶液,前者与后者的c(OH-) | |
| C. | 相同温度下,0.2 mol•L-1醋酸溶液和0.1 mol•L-1醋酸溶液中的c(H+) | |
| D. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积 |
5.室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
| A. | 向0.10mol/L NH4HCO3中溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) | |
| B. | 向0.10mol/L NaHSO3中溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-) | |
| C. | 向0.10mol/L Na2SO3中溶液中通入SO2:c(Na+)=2[c(H2SO3)+c(HSO3-)+c(SO32-)] | |
| D. | 向0.10mol/L CH3COONa中溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-) |
12.下列实验一定不会出现沉淀现象的是( )
| A. | CO2气体通入Na2SiO3溶液中 | B. | CO2气体通入饱和Na2CO3溶液中 | ||
| C. | SO2气体通入BaCl2溶液中 | D. | SO2气体通入Ba(OH)2溶液中 |
9.下列电离方程式正确的是( )
| A. | Ba(OH)2═Ba2++2OH- | B. | AlCl3═Al3++Cl3- | ||
| C. | H2SO4═2H++S6++4O2- | D. | Na2CO3═Na2++CO32- |
10.下列对应化学反应的离子方程式正确的是( )
| A. | KIO3与KI在酸性溶液中反应:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | 向碳酸氢铵溶液中加过量氢氧化钠溶液并加热:NH4++OH-═NH3↑+H2O | |
| C. | Na[Al(OH)4]-溶液中通入过量CO2制Al(OH)3:CO2+[Al(OH)4]-═Al(OH)3↓+HCO3- | |
| D. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O |
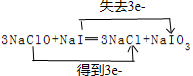 ,还原剂与氧化剂的物质的量之比是1:3.
,还原剂与氧化剂的物质的量之比是1:3.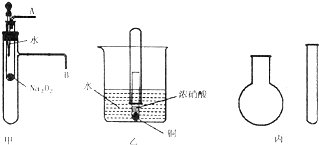 “套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验.因其具有许多优点,已被广泛应用于化学实验中.下列三个实验均为“套管实验”,请观察、分析,回答下列问题:
“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验.因其具有许多优点,已被广泛应用于化学实验中.下列三个实验均为“套管实验”,请观察、分析,回答下列问题: .
.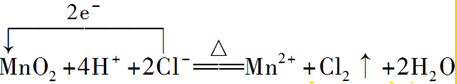 .
.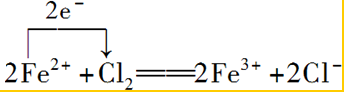 .
.