题目内容
下列实验操作或对实验事实的描述不正确的是( )
| A、不宜用瓷坩埚灼烧氢氧化钠或碳酸钠 |
| B、使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大 |
| C、分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出 |
| D、用托盘天平称量11.74 g氯化钠晶体 |
考点:配制一定物质的量浓度的溶液,分液和萃取
专题:化学实验基本操作
分析:A、瓷坩埚中含二氧化硅,能与碱反应;
B、定容时俯视刻度线,会导致溶液体积偏小;
C、分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出,如果上层液体也从下口放出,会使残留的下层液体又混入上层液体;
D、托盘天平精确到0.1g.
B、定容时俯视刻度线,会导致溶液体积偏小;
C、分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出,如果上层液体也从下口放出,会使残留的下层液体又混入上层液体;
D、托盘天平精确到0.1g.
解答:
解:A、瓷坩埚中含二氧化硅,能与碱反应,则不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体,故A正确;
B、定容时俯视刻度线,会导致溶液体积偏小,则所配制溶液浓度偏大,故B正确;
C、分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出,如果上层液体也从下口放出,会使残留的下层液体又混入上层液体,故C正确;
D、托盘天平只能精确到0.1g,故D错误;
故选D.
B、定容时俯视刻度线,会导致溶液体积偏小,则所配制溶液浓度偏大,故B正确;
C、分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出,如果上层液体也从下口放出,会使残留的下层液体又混入上层液体,故C正确;
D、托盘天平只能精确到0.1g,故D错误;
故选D.
点评:本题考查化学实验方案的评价,涉及固体的熔融、溶液的配制、分液操作等,注意物质的性质与反应原理,题目难度中等.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下22.4LH2O中的分子数为NA |
| B、22.4LCl2所含分子数目为NA |
| C、23gNa变成Na+时失去的电子数目为NA |
| D、2g氢气所含原子数目为NA |
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B、分别加水稀释10倍,四种溶液的pH①>②>④>③ |
| C、①④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、VaL②与VbL③溶液混合后,若混合后溶液pH=7,则Va>Vb |
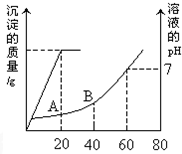
在Al2(SO4)3、K2SO4和KAl(SO4)2的混合溶液中,如果SO42-的物质的量浓度为0.2mol?L-1,当加等体积的0.2mol?L-1的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A、0.2 mol?L-1 |
| B、0.25 mol?L-1 |
| C、0.45 mol?L-1 |
| D、0.225 mol?L-1 |
 (1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=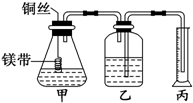 某研究性学习小组为证明在同温同压下,相同浓度、相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度、相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤如下: