题目内容
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B、分别加水稀释10倍,四种溶液的pH①>②>④>③ |
| C、①④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、VaL②与VbL③溶液混合后,若混合后溶液pH=7,则Va>Vb |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:①中c(NH3.H2O)>0.001mol/L,②中c(NaOH)=0.001mol/L③中c(CH3COOH)>0.001mol/L,④中c(HCl)=0.001mol/L,
A.醋酸钠是强碱弱酸盐,其水溶液呈碱性;
B.加水稀释相同的倍数,促进弱电解质电离,导致稀释后弱酸中氢离子浓度大于强酸,弱碱中氢氧根离子浓度大于强碱;
C.pH=3的盐酸浓度小于pH=11的氨水浓度,二者等体积混合氨水有剩余,溶液呈碱性;
D.醋酸为弱酸,c(醋酸)>0.001mol/L,氢氧化钠溶为强电解质,c(氢氧化钠)=0.001mol/L,若溶液为中性,则氢氧化钠的体积一定大于醋酸的体积.
A.醋酸钠是强碱弱酸盐,其水溶液呈碱性;
B.加水稀释相同的倍数,促进弱电解质电离,导致稀释后弱酸中氢离子浓度大于强酸,弱碱中氢氧根离子浓度大于强碱;
C.pH=3的盐酸浓度小于pH=11的氨水浓度,二者等体积混合氨水有剩余,溶液呈碱性;
D.醋酸为弱酸,c(醋酸)>0.001mol/L,氢氧化钠溶为强电解质,c(氢氧化钠)=0.001mol/L,若溶液为中性,则氢氧化钠的体积一定大于醋酸的体积.
解答:
解:①中c(NH3.H2O)>0.001mol/L,②中c(NaOH)=0.001mol/L③中c(CH3COOH)>0.001mol/L,④中c(HCl)=0.001mol/L,
A.醋酸钠是强碱弱酸盐,其水溶液呈碱性,所以③、④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大,故A正确;
B.弱电解质溶液中存在电离平衡,酸或碱加水稀释相同的倍数,弱电解质的pH变化小于强电解质,所以四种溶液的pH①>②>④>③,故B正确;
C.pH=3的盐酸浓度小于pH=11的氨水浓度,二者等体积混合氨水有剩余,溶液呈碱性,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+),否则电荷不守恒,故C错误;
D.由于c(醋酸)>0.001mol/L、c(HCl)=0.001mol/L,若VaL②与VbL③溶液混合后,若混合后溶液pH=7,则必须满足氢氧化钠体积大于醋酸,即Va>Vb,故D正确;
故选C.
A.醋酸钠是强碱弱酸盐,其水溶液呈碱性,所以③、④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大,故A正确;
B.弱电解质溶液中存在电离平衡,酸或碱加水稀释相同的倍数,弱电解质的pH变化小于强电解质,所以四种溶液的pH①>②>④>③,故B正确;
C.pH=3的盐酸浓度小于pH=11的氨水浓度,二者等体积混合氨水有剩余,溶液呈碱性,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+),否则电荷不守恒,故C错误;
D.由于c(醋酸)>0.001mol/L、c(HCl)=0.001mol/L,若VaL②与VbL③溶液混合后,若混合后溶液pH=7,则必须满足氢氧化钠体积大于醋酸,即Va>Vb,故D正确;
故选C.
点评:本题考查弱电解质的电离、酸碱混合溶液定性判断等知识点,根据弱电解质的特点、酸碱混合溶液氢离子浓度的计算方法、电荷守恒进行分析解答,难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、硫酸和磷酸的摩尔质量相等 |
| B、2g氢气中含有1mol氢 |
| C、O2的摩尔质量(单位是g?mol-1)在数值上等于其相对分子质量 |
| D、1molCO的质量是28g?mol-1 |
将0.1mol/L醋酸溶液加水稀释,下列说法正确的是( )
| A、溶液中c(H+)和c(OH-)都减小 |
| B、溶液中c(H+)增大 |
| C、醋酸电离平衡向右移动 |
| D、溶液的pH不变 |
已知H-H键的键能为436kJ/mol,O═O键的键能为498kJ/mol,根据热化学方程式H2(g)+
O2(g)═H2O(l)△H=-286kJ/mol,判断H2O分子中O-H键的键能为( )
| 1 |
| 2 |
| A、485.5 kJ/mol |
| B、610 kJ/mol |
| C、917 kJ/mol |
| D、1 220 kJ/mol |
下列实验操作或对实验事实的描述不正确的是( )
| A、不宜用瓷坩埚灼烧氢氧化钠或碳酸钠 |
| B、使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大 |
| C、分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出 |
| D、用托盘天平称量11.74 g氯化钠晶体 |
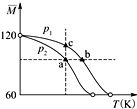 已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )| A、该过程的△H<0 |
| B、气体压强:p(a)<p(b)=p(c) |
| C、平衡常数:K(a)=K(b)<K(c) |
| D、测定乙酸的相对分子质量要在高压、低温条件 |
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶性的甲基磺酸铅为电解质,电池总反应为:Pb+PbO2+4H+
2Pb2++2H2O.下列有关新型液流式铅酸蓄电池的说法正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应式为Pb-2e-+SO42-=PbSO4 |
| B、充放电时,溶液的导电能力变化不大 |
| C、以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L |
| D、充电时的阳极反应式为Pb 2++2e-+4OH-=PbO2+2H2O |
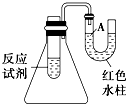 如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:
如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题: