题目内容
16.铵盐是重要的化工原料,以N2和H2为原料制取硝酸铵的流裎阁如下,请回答下列问题:
(1)在上述流程阁中,B设备的名称是氧化炉,其中发生反应的化学方程式为4NH3+5O2 $\frac{\underline{\;Rt-Rh\;}}{△}$4NO+6H2O.
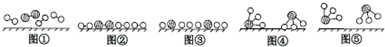
(2)在上述工业生产中,N2与H2合成NH3的傕化剂是铁砂网,1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德.埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示 意图如下:
 、
、 、
、 分别表示N2、H2、NH3图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别 是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂
分别表示N2、H2、NH3图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别 是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂(3)NH3和C02在一定条件下可合成尿素,其反应为:2NH3(g)+CO2(g)?C0(NH2)2(s)+H20(g)
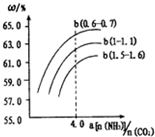
如图表示合成塔中氨碳比a与C02转化率ω的关系a为$\frac{n(N{H}_{3})}{n(C{O}_{2})}$,b 为水碳比$\frac{n({H}_{2}O)}{n(C{O}_{2})}$则:
①b应控制在C
A.1.5~1.6 B.1〜1.1 C.0.6〜0.7
②a应控制在4.0的理由是氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)大于4.0时,增大氨气的物质的量,二氧化碳的转化率增加不大,增加了生产成本;氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)小于4.0时,二氧化碳的转化率较小
(4)在合成氨的设备(合成塔)中,设置热交換器的目的是利用余热,节约能源在合成硝酸的吸收塔中通入空气的目的是使NO循环利用,全部转化为硝酸
(5)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH═2NaNO2+H2O
NH3还原法:8NH3+6NO2$\frac{\underline{\;催化剂\;}}{△}$7N2+12H20 (NO也有类似的反应)
以上两种方法中,符合绿色化学的是氨气还原法
(6)某化肥厂用NH3制备NH4NO3已知:由NH3制NO的产率是96%、NO制HN03的产率是92%.则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的53.1%.
分析 氮气、氢气在合成塔中合成氨气,氨气在氧化炉中氧化为NO,NO、氧气、水吸收塔中合成硝酸,硝酸与氨气合成硝酸铵.
(1)B中发生氨气的催化氧化生成NO,设备为氧化炉;
(2)在上述工业生产中,N2与H2合成NH3的傕化剂是铁砂网;
氮气、氢气在催化剂表面合成氨反应过程的顺序为:图①氮气分子和氢气分子向催化剂表面靠近,图②氮气和氢气吸附在催化剂的表面,图③在催化剂的作用下分解成氢原子和氮原子,在催化剂表面N2、H2中的化学键断裂;图④在催化剂形成NH3;图⑤脱离催化剂表面;
(3)①氨碳比一定时,选择二氧化碳转化率最大时的碳水比;
②氨碳比a大于4.0时,增大氨气的物质的量,二氧化碳的转化率增加不大,增加了生产成本,氨碳比a小于4.0时,二氧化碳的转化率较小;
(4)合成氨为放热反应,温度太高不利于氨气生成,并进行原料气的预热,充分利用余热,节约能源;
在合成硝酸的吸收塔中通入空气,使NO循环利用,全部转化为硝酸;
(5)根据反应化学方程式反应物和生成物的性质和经济效益分析,绿色化学为无污染,原子利用率高的生产;
(6)假设硝酸铵的物质的量为1mol,则与硝酸反应的氨气为1mol,根据原子守恒计算制备硝酸的氨气,每一步损失率、利用率都以氨气计算.
解答 解:(1)氨气在氧化炉中被催化氧化,B设备的名称是氧化炉;氨气被氧化为NO和水,其反应的方程式为:4NH3+5O2 $\frac{\underline{\;Rt-Rh\;}}{△}$4NO+6H2O;
故答案为:氧化炉;4NH3+5O2 $\frac{\underline{\;Rt-Rh\;}}{△}$4NO+6H2O;
(2)N2与H2合成NH3所用的催化剂是铁砂网;氮气、氢气在催化剂表面合成氨反应过程的顺序为:图①氮气分子和氢气分子向催化剂表面靠近,图②氮气和氢气吸附在催化剂的表面,图③在催化剂的作用下分解成氢原子和氮原子,在催化剂表面N2、H2中的化学键断裂;图④在催化剂形成NH3;图⑤脱离催化剂表面;
故答案为:铁砂网;N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂;
(3)①氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)相同时,水碳比($\frac{n({H}_{2}O)}{n(C{O}_{2})}$)为0.6~0.7时,二氧化碳转化率最大,
故答案为:c;
②氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)大于4.0时,增大氨气的物质的量,二氧化碳的转化率增加不大,增加了生产成本;氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)小于4.0时,二氧化碳的转化率较小,
故答案为:氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)大于4.0时,增大氨气的物质的量,二氧化碳的转化率增加不大,增加了生产成本;氨碳比a($\frac{n(N{H}_{3})}{n(C{O}_{2})}$)小于4.0时,二氧化碳的转化率较小;
(4)合成氨的反应属于放热反应,反应过程中会放出大量的热,用热交换器并进行原料气的预热,可以充分利用余热,节约能源,还有利于氨气的生成;在吸收塔中二氧化氮与水反应生成硝酸和NO,通入空气,NO能被空气中的氧气氧化为二氧化氮,二氧化氮再与水反应生成硝酸,这样使NO循环利用,全部转化为硝酸;
故答案为:利用余热,节约能源;使NO循环利用,全部转化为硝酸;
(4)碱液吸收法:NO+NO2+2NaOH═2NaNO2+H2O,NH3还原法:8NH3+6NO2 $\frac{\underline{催化剂}}{△}$7N2+12H2O,分析可知碱液吸收法消耗大量的氢氧化钠生成的亚硝酸盐毒,NH3还原法产物无污染,得到合成氨的原料气,故符合绿色化学的是氨气还原法;
故答案为:氨气还原法;
(5)假设硝酸铵的物质的量为1mol,则与硝酸反应的氨气为1mol,制备的硝酸为1mol,令制备硝酸的氨气为xmol,每一步损失率、利用率都以氨气计算,根据原子守恒,xmol×96%×92%=1mol,解得x=$\frac{10000}{96×92}$%,故制HNO3所用去的氨气的质量占总耗氨的质量分数是$\frac{\frac{10000}{96×92}mol}{1mol+\frac{10000}{96×92}mol}$×100%≈53.1%,
故答案为:53.1%.
点评 本题考查化学工业制备、阅读获取信息的能力、化学计算等,(6)中注意利用守恒思想计算,也可以利用关系式计算,是对学生综合能力的考查.

| A. | 用量筒测得排水法收集制得的氢气体积为5.28 mL | |
| B. | 用两只250 mL的容量瓶配制0.1mol/L 500 mL的NaOH溶液 | |
| C. | 用托盘天平称得2.50g胆矾,受热充分失水后,固体质量减轻0.90g | |
| D. | 常温下,测得1molN2的质量为28g |
Ⅰ.制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.9 | 8.9 |
| Fe2+ | 5.8 | 8.8 |
(1)为了加快反应,“酸溶”需要适当加热,但是温度不宜太高,原因是防止金属离子水解形成沉淀,以及温度过高H2O2发生分解.
(2)沉淀A的化学式为Cu.
(3)调节pH的范围为3.2≤pH<5.2;若试剂X为Zn2(OH)2CO3,加人X除杂质的离子方程为Zn2(OH)2CO3+4H+=2Zn2++3H2O+CO2↑.
| A. | 简单离子半径:X<Y<W | |
| B. | Y、Z两种元素的氧化物均具有两性 | |
| C. | X、W分别形成的氢化物中所含化学键种类相同 | |
| D. | Z、W形成化合物的电子式为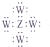 |
| A. | 元素的非金属性:N<O<F | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 热稳定性:HF>HCl>H2S | D. | 原子半径:Al>Mg>Na |

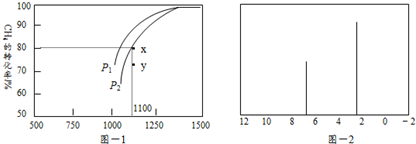
| A. | 金属Mg采用②堆积方式 | |
| B. | ①和③中原子的配位数分别为:8、12 | |
| C. | 对于采用②堆积方式的金属,实验测得W g该金属的体积为V cm3,则阿伏加德罗常数NA的表达式为$\frac{MV}{W•(\frac{4}{\sqrt{3}}r)^{3}}$ | |
| D. | ④中空间利用率的表达式为:$\frac{\frac{4}{3}π{r}^{3}×4}{(\frac{4}{\sqrt{2}}r)^{3}}$×100% |
| A. | 天然气用做燃料 | B. | 无水乙醇直接用作医用消毒 | ||
| C. | 苯酚用于制杀菌剂 | D. | 福尔马林用于浸制生物标本 |
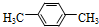 .
.