题目内容
 利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )
利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )| 选项 | 实验目的 | 甲 | 乙 | 丙 |
| A | 制取并收集NH3 | 浓氨水 | CaO | H2O |
| B | 制取并验证C2H2可被KMnO4酸性溶液氧化 | 饱和食盐水 | 电石 | KMnO4酸性溶液 |
| C | 制取并验证Cl2没有漂白性 | 浓盐酸 | MnO2 | 干燥的红布条 |
| D | 制取并验证SO2具有漂白性 | 70%硫酸 | Na2SO3 | 品红试液 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氨气易溶于水,不能用排水法收集;
B.实验室制备乙炔,气体中混有硫化氢等杂质;
C.氯气不能使干燥的有色布条褪色;
D.70%硫酸与Na2SO3反应生成二氧化硫,可使品红褪色.
B.实验室制备乙炔,气体中混有硫化氢等杂质;
C.氯气不能使干燥的有色布条褪色;
D.70%硫酸与Na2SO3反应生成二氧化硫,可使品红褪色.
解答:
解:A.氨气易溶于水,应用向下排空法收集,不能用排水法收集,故A错误;
B.实验室制备乙炔,气体中混有硫化氢等杂质,与酸性高锰酸钾发生氧化还原反应,应先除杂,故B错误;
C.氯气不能使干燥的有色布条褪色,故C错误;
D.70%硫酸与Na2SO3反应生成二氧化硫,可使品红褪色,可用该装置制取并验证SO2具有漂白性,故D正确.
故选D.
B.实验室制备乙炔,气体中混有硫化氢等杂质,与酸性高锰酸钾发生氧化还原反应,应先除杂,故B错误;
C.氯气不能使干燥的有色布条褪色,故C错误;
D.70%硫酸与Na2SO3反应生成二氧化硫,可使品红褪色,可用该装置制取并验证SO2具有漂白性,故D正确.
故选D.
点评:本题考查较为综合,涉及气体的制取以及性质检验,为高频考点,侧重学生的分析、实验能力的考查,注意把握物质的性质,难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
三聚氯氰是叫种重要的精细化工产品,广泛用于制造农药、染料、炸药、医药等工业.目前工业上生产三聚氯氰的反应原理为:3NaCN+3Cl2
3NaCl+ 下列有关说法正确的是( )
下列有关说法正确的是( )
| 活性炭 |
| 400℃ |
 下列有关说法正确的是( )
下列有关说法正确的是( )| A、三聚氯氰中C1的化合价是+1 |
| B、该反应中NaCN被还原 |
| C、三聚氯氰分子中既含σ键又含π健 |
| D、36.9 g三聚氯氰中含有1.204×1023个原子 |
 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )| 选项 | 发生装置中的药品 | 干燥和集气装置 |
| A | 亚硫酸钠和稀盐酸 | 图2 |
| B | 大理石和稀盐酸 | 图1 |
| C | 铜和稀硝酸 | 图2 |
| D | 氧化钙和浓氨水 | 图1 |
| A、A | B、B | C、C | D、D |
某溶液中可能含有K+、NH4+、Ba2+、SO42-、I-、Cl-、NO3-中的几种,将此溶液分成两等份,进行如下实验:
①在一份溶液中加入足量NaOH,加热,可收集到标准状态下的气体1.12L;
②在另一份溶液中加入足量Ba(NO3)2溶液,有白色沉淀产生,过滤得到沉淀2.33g;
③在②的滤液中加入足量AgNO3溶液,又有4.7g沉淀产生.
有关该溶液中离子种类(不考虑H+和OH-)的判断正确的是( )
①在一份溶液中加入足量NaOH,加热,可收集到标准状态下的气体1.12L;
②在另一份溶液中加入足量Ba(NO3)2溶液,有白色沉淀产生,过滤得到沉淀2.33g;
③在②的滤液中加入足量AgNO3溶液,又有4.7g沉淀产生.
有关该溶液中离子种类(不考虑H+和OH-)的判断正确的是( )
| A、溶液中至少有2种阳离子 |
| B、只能确定溶液中NH4+、SO42-是否存在 |
| C、溶液中最多有4种阴离子 |
| D、溶液中不可能同时存在K+和NO3- |
下列说法正确的是( )
| A、除去NO中混有的NO2将混合气体先通过足量水,然后用CaCl2干燥 |
| B、配制一定物质的量浓度的Fe(NO3)2溶液:将一定量的Fe(NO3)2溶于适量的硝酸中,再加入水稀释至指定浓度 |
| C、向足量饱和石灰水中加入少CaO,恢复至室温后溶液pH变大 |
| D、工业上分別用电解熔融Al2O3、MgO、NaCl的方法制取Al、Mg、Na |
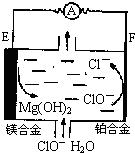 镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔.如图为“镁一次氯酸盐”燃料电池示意图,电极为镁合金和铂合金.关于该电池的叙述正确的是( )
镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔.如图为“镁一次氯酸盐”燃料电池示意图,电极为镁合金和铂合金.关于该电池的叙述正确的是( )| A、E为该燃料电池的正极 |
| B、负极发生的电极反应式为ClO-+2e-+H2O=Cl-+2OH- |
| C、电池工作时,正极周围溶液的pH将不断变小 |
| D、镁燃料电池负极能发生自腐蚀产生氢气,使负极利用率降低 |
 Z(g)+M(s),5min后达到平衡,此时生成a mol Z。下列说法正确的是
Z(g)+M(s),5min后达到平衡,此时生成a mol Z。下列说法正确的是 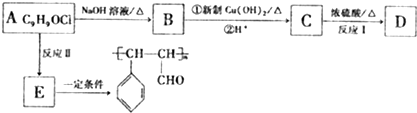
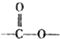 结构的芳香族化介物的同分异构体有
结构的芳香族化介物的同分异构体有 6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题: