题目内容
19.下列各装置不能构成原电池的是(电解质溶液均为稀硫酸)( )| A. |  | B. | 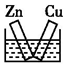 | C. | 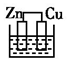 | D. |  |
分析 原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,以此来解答.
解答 解:A.锌比Cu活泼,二者接触,并插入电解质溶液中,锌失电子,溶液中氢离子在铁电极上得电子,能构成原电池,故A不选;
B.Zn比Cu活泼,二者接触,并插入电解质溶液中,Zn失电子,溶液中氢离子在铜电极上得电子,能构成原电池,故B不选;
C.Zn比Cu活泼,二者接触,并插入电解质溶液中,Zn失电子,溶液中氢离子在铜电极上得电子,能构成原电池,故C不选;
D.没有构成闭合回路,所以不能构成原电池,故D选;
故选D.
点评 本题考查原电池,为高频考点,把握原电池的构成条件为解答的关键,侧重分析与应用能力的考查,注意原电池的工作原理,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.水溶液X中只可能溶有Na+、Ca2+、Fe3+、[Al(OH)4]-、SiO32-、CO32-、SO42-中的若干种离子.某同学对该溶液迸行了如下实验:下列判断正确的是( )
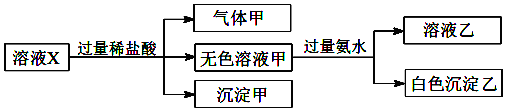

| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸钙的混合物 | |
| C. | CO32-和SO42-一定不存在于溶液X中 | |
| D. | Na+、[Al(OH)4]-和SiO32-一定存在于溶液X中 |
10.下列表述错误的是( )
| A. | C3H8分子中的碳原子一定不在同一直线上 | |
| B. | 乙酸与乙醇反应的化学方程式:CH3COOH+C2H518OH$?_{△}^{浓H_{2}SO_{4}}$CH3CO18OC2H5+H2O | |
| C. | 用溴水不能区分植物油和矿物油,也不能区分CCl4和苯 | |
| D. | 分子式为C5H12O的有机物在Cu的催化作用下发生催化氧化,但产物不能发生银镜反应的有(不考虑立体异构)3 种 |
14.元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )
| A. | 元素原子的最外层电子数等于元素的最高化合价 | |
| B. | 只含共价键的物质一定是共价化合物 | |
| C. | P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
4.分子式为C5H9Br的有机物,其结构可能是( )
| A. | 只含有2个双键的直链有机物 | B. | 含1个双键的直链有机物 | ||
| C. | 含1个双键的环状有机物 | D. | 含一个三键的直链有机物 |
11.根据下列操作、预期现象和所得结论正确的是( )
| 操作及预期现象 | 结论 | |
| A | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| B | 向某无色溶液滴加硝酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | A1箔插入稀HNO3中,无现象 | A1箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 原溶液中有Na+无K+ |
| A. | A | B. | B | C. | C | D. | D |